░l▓╝╚šŲ┌Ż║2026-2-22 9:52:09
ļSų°╣Ū┐Ų╝▓▓Ī░l▓Ī┬╩▓╗öÓ╔Ž╔²╝░Š½£╩ßtīW└Ē─ŅĄ─╔Ņ╚ļ░lš╣Ż¼┼R┤▓ī”éĆąį╗»ĪóĖ▀Ųź┼õČ╚╣Ū┐Ųų▓╚ļ╬’Ą─ąĶŪ¾╚šęµŲ╚ŪąĪŻŌü║ŽĮæ{ĮĶŲõĖ▀ÅŖČ╚Īóā×┴╝╔·╬’ŽÓ╚▌ąį║═─═Ė»╬gąį─▄Ż¼ķLŲ┌š╝ō■╣Ū┐Ųų▓╚ļ▓─┴ŽĄ─ų„ī¦Ąž╬╗Ż¼Ą½é„ĮyųŲįņ╝╝ągį┌Å═ļsĮŌŲ╩ĮYśŗ│╔ą╬ĪóéĆ¾w╗»Ųź┼õ╝░╬óė^ĮYśŗŠ½£╩š{┐žĘĮ├µųØu▒®┬Č│÷ŠųŽ▐ąįĪŻĮ³─ĻüĒŻ¼▀xģ^╝ż╣Ō╚█╗» (SLM) ║═ļŖūė╩°╚█╗» (EBM) Ą╚į÷▓─ųŲįņ╝╝ągę└═ąöĄūų╗»įOėŗ║═ųīė│╔ą╬ÖCųŲŻ¼īŹ¼F┴╦ČÓ┐ūĮYśŗĪó╣”─▄╠▌Č╚▓─┴Ž╝░Å═ļsÄū║╬¾wĄ─Š½┤_śŗų■Ż¼į┌Ė─╔Ų┴”īWŲź┼õąį║═┤┘▀M╣Ūš¹║ŽĘĮ├µ▒Ē¼F│÷’@ų°ā×ä▌Ż¼Ą½į┌▒Ē├µ┤ų▓┌Č╚┐žųŲ╝░┐ūŽČĮYśŗ┼c┴”īWąį─▄Ą─ģf═¼ā×╗»ĘĮ├µ╚į├µ┼R╠¶æĪŻį┌┤╦╗∙ĄA╔ŽŻ¼╚╦╣żųŪ─▄▒╗ę²╚ļŌü║ŽĮį÷▓─ųŲįņ┼c╣Ū┐Ųų▓╚ļ▓─┴ŽčąŠ┐ųąŻ¼ū„×ķž×┤®įOėŗ - ųŲįņ - įuār - ┼R┤▓ŅA£y╚½▀^│╠Ą─║╦ą─╣żŠ▀Ż║į┌įOėŗļAČ╬Ż¼AI ═©▀^═žōõā×╗»┼c╔·│╔╩Į╦ŃĘ©īŹ¼F▌p┴┐╗»ĪóČÓ┐ū╝░╠▌Č╚╗»ĮYśŗįOėŗŻ¼ęįŠÅĮŌÅŚąį─Ż┴┐╩¦┼õ║═æ¬┴”š┌ō§Ż╗į┌ųŲįņļAČ╬Ż¼ÖCŲ„īW┴Ģ┼c╔ŅČ╚īW┴Ģė├ė┌īŹĢr▒O£y SLM ▀^│╠ųąĄ─╚█│ž╝░ČÓ╬’└Ēą┼╠¢Ż¼īŹ¼F╚▒Ž▌ūRäe┼c╣ż╦ćūį▀m欚{┐žŻ╗į┌įuār┼cæ¬ė├īė├µŻ¼AI īó SLM ųŲéõĄ─ Ti-6Al-4V (Ti64) īŹ“×öĄō■┼cėąŽ▐į¬┴”īW - ╔·╬’īW╣Ūė·║Ž─Żą═ŽÓĮY║ŽŻ¼Įę╩ŠĮYśŗ - ąį─▄ - ╣Ūė·║Žų«ķgĄ─ĘŪŠĆąįĻPŽĄŻ¼īŹ¼F╣Ūį┘╔·┼cķLŲ┌ĘĆČ©ąįĄ─┐ņ╦┘ŅA£yŻ¼Å─Č°═ŲäėŌü║ŽĮ╣Ū┐Ųų▓╚ļ╬’Ž“ųŪ─▄╗»Ī󊽣╩╗»║═éĆąį╗»ĘĮŽ“░lš╣ĪŻ▒Š╬─ŽĄĮyĄž╩ß└ĒŌü║ŽĮį÷▓─ųŲįņį┌╣Ū┐ŲųąĄ─æ¬ė├蹊┐▀Mš╣Ż¼▒╚▌^▓╗═¼╝╝ąg┬ĘŠĆĄ─ā×┴ėŻ¼ų╝į┌×ķŽ┬ę╗┤·ų▓╚ļ╬’Ą─äōą┬įOėŗ┼c┼R┤▓▐D╗»╠ß╣®ę└ō■Ż¼═Ųäė╣Ū┐Ųų▓╚ļ▓─┴ŽĄ─╝╝ągĖ’ą┬┼c┼R┤▓æ¬ė├═žš╣ĪŻ
1ĪóŌü║ŽĮ▓─┴Ž╠žąį┼c╣Ū┐Ų▀m┼õąį
1.1 ┴”īWŲź┼õąį
Ti6A14V (E≈110 GPa) ę“ÅŖČ╚ā׫É▒╗ÅVĘ║ė├ė┌╣Ū┐Ųų▓╚ļŻ¼Ą½ŲõäéČ╚╝s×ķŲż┘|╣Ū (10~30GPa) Ą─ 3~10 ▒ČŻ¼▓╗┐╔▒▄├ŌĄžę²░læ¬┴”š┌▒╬ĪŻų▓╚ļ╬’│ąō·┤¾▓┐Ęų▌d║╔║¾Ż¼ų▄ć·╣Ūæ¬ūā¾EĮĄŻ¼ķLŲ┌ī¦ų┬╣Ū┴┐üG╩¦Īó╬³╩š╝░¤oŠ·ąį╦╔äėĪŻ×ķ┐sąĪ─Ż┴┐▓ŅŠÓŻ¼čąŠ┐═¼▓Į═Ų▀M│╔ĘųįOėŗ┼cĮYśŗ╣ż│╠Ż¼ų„ę¬╝╝ąg▓▀┬į░³└©║ŽĮ╗»╠Ä└Ē╗∙¾w║═ČÓ┐ū╗»ĮYśŗįOėŗā╔ĘĮ├µĪŻ(1) ║ŽĮ╗»Ż║╠Ē╝ė NbĪóZr Ą╚ β ĘĆČ©į¬╦ž┐╔½@Ą├å╬ę╗ β ŽÓŻ¼’@ų°ĮĄĄ═ÅŚąį─Ż┴┐ĪŻOzan Ą╚ł¾Ą└Ą─ Ti–Nb–Zr ║ŽĮ E=62 ~ 65 GPaŻ¼Ū³Ę■ÅŖČ╚ 700MPa ╝ēŻ¼čė╔ņ┬╩ > 10%Ż¼ÅŚąįæ¬ūā 1.31%Ż╗Ė▀ Zr ║¼┴┐▀ĆęųųŲ┴ū╦ßŌ}▀^Č╚│┴ĘeŻ¼ŠS│ų│╔╣Ū╝Ü░¹╗ŅąįŻ¼╝µŅÖæ¬┴”š┌▒╬ŠÅĮŌ┼c║¾Ų┌╚Ī│÷ąĶŪ¾ĪŻ(2) ČÓ┐ū╗»Ż║═©▀^į÷▓─ųŲįņš{┐ž┐ūŽČ┬╩┐╔▀Mę╗▓ĮŽ┬š{▒Ēė^─Ż┴┐ĪŻDevaraj Ą╚▓╔ė├ SLM ųŲéõ┐ūŽČ┬╩ 20~40% Ą─ Ti6Al4VŻ¼30% ┐ūŽČįćśė E≈60GPaŻ¼┼c╦╔┘|╣ŪĮėĮ³ĪŻMurr Ą╚└¹ė├ EBM śŗĮ© 60~80% ┐ūŽČĮYśŗŻ¼─Ż┴┐ĮĄų┴ 40~80GPaŻ¼═¼Ģr╠ß╣®╚²ŠS╗ź═©┐šķgŻ¼└¹ė┌╣ŪķL╚ļ┼cč¬╣▄╗»Ż¼┤┘▀M╣Ūš¹║ŽĪŻŠC╔ŽŻ¼│╔Ęų - ĮYśŗģf═¼▓▀┬į┐╔īóŌü║ŽĮėąą¦─Ż┴┐š{ų┴╣Ū╦«ŲĮŻ¼×ķķ_░l┴”īW - ╔·╬’īWąį─▄╝µāץ─ą┬ę╗┤·ų▓╚ļ╬’╠ß╣®┐╔ąą═ŠÅĮĪŻ
1.2 ╔·╬’ŽÓ╚▌ąį
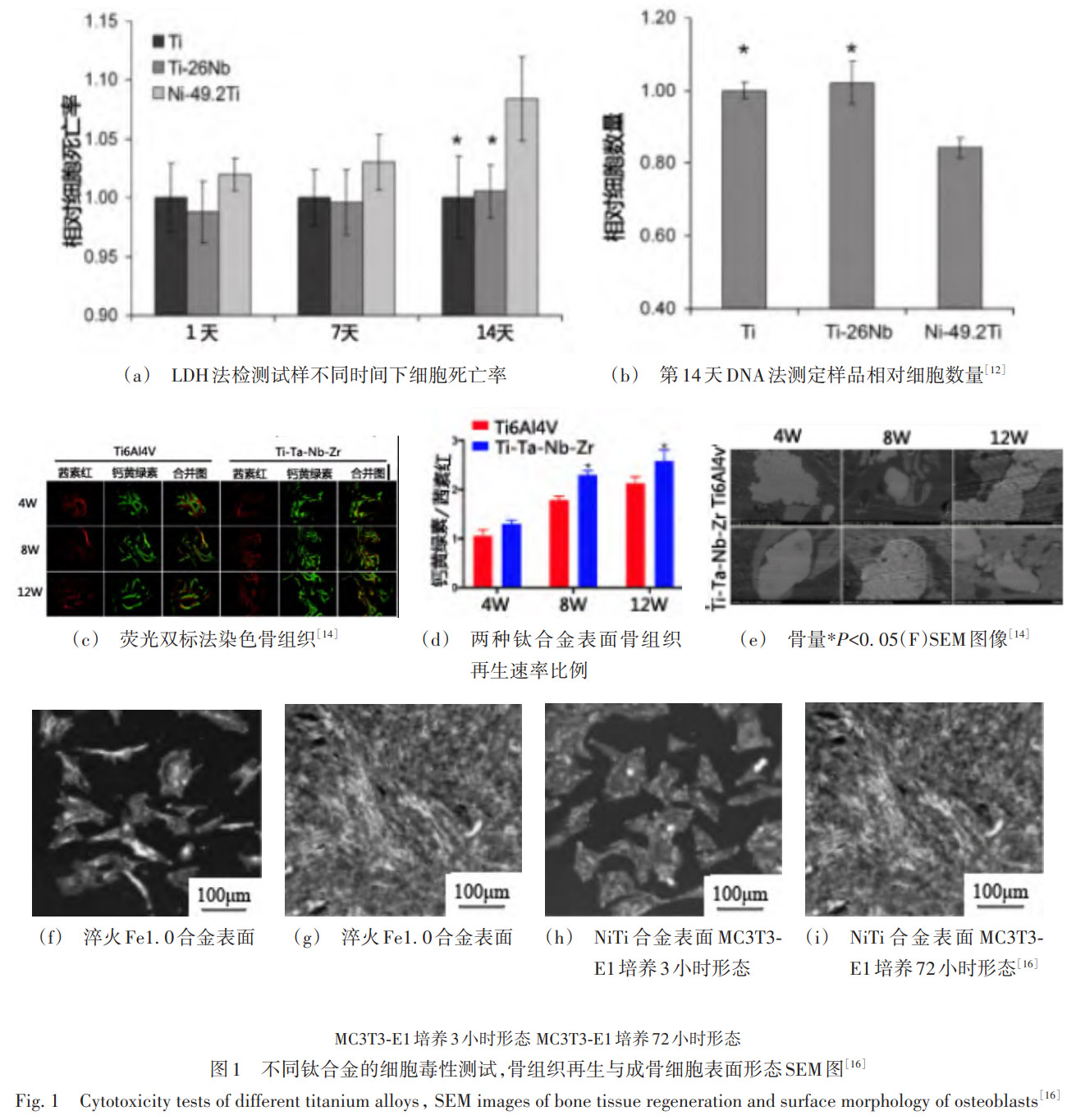
Ōü║ŽĮĄ─╣Ū┤▓æ¬ė├Ė∙╗∙į┌ė┌Ųõū┐įĮĄ─╔·╬’ŽÓ╚▌ąįŻ║▓╗āH┐╔ęÄ▒▄╦▐ų„├Ōę▀┼┼│ŌŻ¼▀Ć─▄ų„äėšTī¦╣ŪįŁ╝Ü░¹ĖĮų°┼cŽ“ą─ąįķL╚ļĪŻ×ķ┴╦═╗ŲŲ Ti6Al4V ╣╠ėąąį─▄Ą─śOŽ▐Ż¼Į³Ų┌蹊┐▓╔ė├ “│╔Ęų - ĮYśŗ - ▒Ē├µ” ╚²į¬ģf═¼▓▀┬įŻ¼ŽĄĮy╠ß╔²╣Ūš¹║Žą¦┬╩ĪŻMcMahon Ą╚į┌ŽĄĮy▒╚▌^┴╦ Ni-49.2Ti ┼c Ti-26Nb ą╬ĀŅėøæø║ŽĮĄ─╝Ü░¹ŽÓ╚▌ąį┼c─═Ė»╬gąą×ķŻ¼▓╔ė├╚²ŠS PEGDA ╦«─² ─z░³┬± NIH3T3 │╔└wŠS╝Ü░¹Ą─ķgĮė¾w═Ō┼ÓB─Żą═Ż¼═©▀^╚ķ╦ß├ōÜõ├Ė (LDH) ßīĘ┼┼c DNA ║¼┴┐įu╣└╝Ü░¹ČŠąįŻ¼═¼ĢrĮY║ŽļŖ╗»īWäėļŖ╬╗śO╗»£yįćĪóICP-MS ļxūėßīĘ┼Ęų╬÷╝░ SIMS ▒Ē├µ│╔Ęų╔ŅČ╚Ų╩╬÷Ż¼╚½├µ▒Ēš„▓─┴Žį┌ŅÉ╔·└ĒŁhŠ│ųąĄ─Ę┤æ¬ąą×ķĪŻčąŠ┐ĮY╣¹’@╩ŠŻ¼Ti-26Nb ║ŽĮį┌š¹éĆ┼ÓBų▄Ų┌ā╚Ą─╝Ü░¹ČŠąį╦«ŲĮ┼c╝āŌüŽÓ«öŻ¼Č° NiTi ║ŽĮį┌ķLŲ┌┼ÓB (14d) ║¾▒Ē¼F│÷Ė³Ė▀Ą─ LDH ßīĘ┼║═’@ų°ĮĄĄ═Ą─ DNA ║¼┴┐Ż¼’@╩Š│÷▌^ÅŖĄ─╝Ü░¹ČŠąįĪŻįō▓Ņ«Éų„ę¬Üwę“ė┌ NiTi ║ŽĮ▌^Ė▀Ą─µćļxūėßīĘ┼║═▌^Ą═Ą──═Ė»╬gĘĆČ©ąįŻ╗ŽÓ▌^ų«Ž┬Ż¼Ti-26Nb ║ŽĮė╔ė┌ Ti ┼c Nb Š∙─▄ą╬│╔ĘĆČ©Ą─Ōg╗»č§╗»─żŻ¼Ųõļxūė╚▄│÷’@ų°ĮĄĄ═Īó─═╬gąįĖ³āׯ¼Å─Č°▒Ē¼F│÷Ė³║├Ą─╔·╬’ŽÓ╚▌ąįĪŻLiu Ą╚└¹ė├╝ż╣ŌĘ█─®┤▓╚█╚┌ (LPBF) īŹ¼F Ti-Ta įŁ╬╗║ŽĮ╗»Ż¼╦∙Ą├▓─┴ŽŲŻä┌śOŽ▐▌^╝āŌü╠ß╔² 35%Ż╗═├╣╔╣Ū╚▒ōp─Żą═ 12 ų▄║¾╣Ū - ų▓╚ļ╬’Įėė|┬╩ (BIC) ▀_ 40%Ż¼×ķ╝āŌüĮM 1.9 ▒ČŻ¼ŅA╩Šā׫ɥ─┼R┤▓▐D╗»æ¬ė├Ū░Š░ĪŻGuo Ą╚═©▀^▀xģ^╝ż╣Ō╚█╗» (SLM) śŗų■┐ūŽČ┬╩ 60%Īó┐ūÅĮ 300~400µ Ą─ Ti-Ta-Nb-Zr ų¦╝▄Ż¼▒Ēė^─Ż┴┐ĮĄų┴ 2.34GPaŻ¼┼c╦╔┘|╣ŪĖ▀Č╚Ųź┼õŻ╗¾w═ŌīŹ“×’@╩ŠŻ¼╚╦╣Ū╦Ķķg│õ┘|Ė╔╝Ü░¹ (hBMSCs) į┌Ųõ▒Ē├µżĖĮ┬╩╠ßĖ▀ 30%Ż¼ALP ╗Ņąį╠ß╔² 1.8 ▒ČŻ╗═├╣╔╣Ū„┴╚▒ōp 12 ų▄ą┬╣Ū¾wĘeĘųöĄ▀_ 45%Ż¼ūCīŹ═¼▓ĮĮĄĄ═æ¬┴”š┌▒╬▓ó╝ė╦┘╣Ūš¹║ŽĪŻJing Ą╚ät▓╔ė├ PLGA - ą┴Ęź╦¹═Ī╦«─²─z═┐īėĖ▓ė┌ SLM Ōüų¦╝▄Ż¼21 ╠ņ└█ėŗßīĘ┼Ż¼Įø TF / NOX₂═©┬ĘšTī¦╣Ū╚Ō┴÷╝Ü░¹Ą“═÷┬╩ 65%Ż¼═¼Ģr╩╣ hBMSCs Ō}ĮY╣Ø│┴Ęeį÷╝ė 50%Ż¼┤¾╩¾╣╔╣ŪĖą╚Š┬╩ė╔ 30% ĮĄų┴ 5%ĪŻXue Ą╚ć·└@Ōü║ŽĮį┌╚╦¾wųąĄ─╔·╬’ŽÓ╚▌ąįå¢Ņ}Ż¼ųŲéõ▓óŽĄĮy蹊┐┴╦ę╗ĘN¤oµć│¼ÅŚąį Ti-19Zr-10Nb-1Fe ║ŽĮĪŻ═©▀^║ŽĮ╚█¤Æ┼c¤ß╠Ä└Ē½@Ą├ β ą═ĮM┐ŚŻ¼▓╔ė├ļŖ╗»īWśO╗»£yįć║═ļxūėßīĘ┼īŹ“×įu╣└Ųõį┌─ŻöM¾wę║ųąĄ──═Ė»╬gąą×ķ┼cĮī┘ļxūė╚▄│÷╠žąįŻ¼▓óĮY║Ž│╔╣Ū╝Ü░¹¾w═Ō┼ÓBīŹ“×Īó╚▄č¬īŹ“×╝░謹Ī░ÕżĖĮ / ╝ż╗Ņ£yįćŻ¼╚½├µ▒Ēš„Ųõ╝Ü░¹ŽÓ╚▌ąį┼cč¬ę║ŽÓ╚▌ąįĪŻĮY╣¹▒Ē├„Ż¼įōŌü║ŽĮį┌ Hank’s ╚▄ę║ųą▒Ē¼F│÷Ė³Ą═Ą─Ė»╬g╦┘┬╩║═’@ų°ĮĄĄ═Ą─ļxūėßīĘ┼┴┐Ż¼│╔╣Ū╝Ü░¹żĖĮ┼cį÷ų│ąį─▄┼c NiTi ║ŽĮŽÓ«öŻ¼Ą½į┌╚▄č¬┬╩║═謹Ī░Õ╝ż╗Ņ│╠Č╚ĘĮ├µ├„’@ā×ė┌ NiTiĪŻĄ├│÷ĮYšō Ti-19Zr-10Nb-1Fe ║ŽĮæ{ĮĶĄ═ČŠį¬╦žĮM│╔Īóā×┴╝─═╬gąį╝░┴╝║├Ą─╝Ü░¹┼cč¬ę║ŽÓ╚▌ąįŻ¼š╣¼F│÷ū„×ķą┬ę╗┤·Ė▀╔·╬’ŽÓ╚▌ąįßtė├Ōü║ŽĮĪó╠µ┤·é„Įy NiTi ║ŽĮĄ─Øōį┌æ¬ė├ārųĄĪŻLi Ą╚įOėŗ 55% ┐ūŽČ┬╩Ą─ĘĮą╬ŚUĀŅČÓ┐ū Ti6Al4VŻ¼ėŗ╦Ń┴„¾wäė┴”īW▒Ē├„Ųõ╝¶Ūąæ¬┴”═©▀^ Piezo1/YAP ą┼╠¢▌S’@ų°┤┘▀Mį÷ų│ (7 ~d OD ≈1.8)ĪŻē║┐sÅŖČ╚╝s 280MPa ĮėĮ³Ųż┘|╣ŪŻ╗═├ŽźĻP╣Ø╚▒ōp 12 ų▄▄ø╣Ūīė║±Č╚▀_ 0.8mmŻ¼▌^Š∙┐ūų¦╝▄į÷║± 30%ĪŻŠC╔ŽŻ¼│╔Ęųā×╗»ĪóČÓ╝ē┐ūĮYśŗ╝░╦Ä╬’ŠÅßī═┐īėĄ─ģf═¼╝»│╔Ż¼╩╣ą┬ę╗┤·Ōü║ŽĮų▓╚ļ╬’į┌┴”īW▀m┼õĪó╣Ūš¹║Ž╦┘┬╩┼c┐╣Ėą╚Šąį─▄╔ŽīŹ¼F═¼▓Į▄S╔²Ż¼×ķÅ═ļs╣Ū┐Ų╚▒ōpą▐Å═╠ß╣®┴╦śOŠ▀ĖéĀÄ┴”Ą─ŠC║ŽĮŌøQĘĮ░ĖĪŻ
1.3 ─═Ė»╬gąį
Ōü║ŽĮ▒Ē├µūį░l╔·│╔Ą─╝{├ū╝ē TiO₂č§╗»─ż┘xėĶŲõį┌╔·└ĒŁhŠ│ųąā׫ɥ─╗»īWĘĆČ©ąįŻ¼ķLŲ┌Ę■ę█╚į▒Ż│ųĄ═Ė»╬g╦┘┬╩ĪŻ×ķ┴╦▀Mę╗▓Į╠ß╔²─═╬gśOŽ▐Ż¼▒Ē├µĖ─ąįęč│╔×ķĻPµI═╗ŲŲ┐┌ĪŻChelappa Ą╚▓╔ė├ļŖėŠ│┴Ęe╝╝ągį┌▒Ē├µśŗų■ SiO₂-ZnO Å═║Ž═┐īėŻ¼▓óęį I₂PVP ģf═¼ų┬├▄╗»ĮYśŗŻ╗─ŻöM¾wę║ųąŻ¼═┐īė╩╣Ė»╬gļŖ╬╗╔²ų┴Ż¼Ė»╬gļŖ┴„├▄Č╚ĮĄų┴ 5.1 ×10⁻² m・A・cm⁻²Ż¼─═╬gąį’@ų°╠ßĖ▀Ż¼Ūę═┐īė╗∙¾wĮY║ŽÅŖČ╚▀_ 45MPaŻ¼═├╣╔╣Ūų▓╚ļ 6 ų▄║¾Įń├µ╣Ūš¹║Ž┬╩╠ß╔² 25%ĪŻXie Ą╚░l¼FŻ¼3D ┤“ėĪ Ti6Al4V ▒Ē├µĄ─▓┐Ęų╚█╗»Ņw┴Ż (PMCs) ŲŲē─č§╗»─ż═Ļš¹ąįŻ¼Cl⁻ØB═Ė╦┘┬╩╠ßĖ▀Ż¼Ė»╬gļŖ┴„├▄Č╚į÷ų┴ 1.8 ×10⁻⁶ A・cm⁻²(×ķ¤o PMCs ▒Ē├µĄ─ 2.3 ▒Č)Ż╗īó╝ż╣Ō╣”┬╩Å─ 180W ╠ßĖ▀ų┴ 220W ║¾Ż¼PMCs ├µĘeĘųöĄė╔ 12% ĮĄų┴ 3%Ż¼³c╬gļŖ╬╗ūį 0.6V ╔²ų┴ 1.1VŻ¼─═╬gąį─▄╗ųÅ═ĪŻGuo Ą╚└¹ė├ 3D ┤“ėĪųŲéõ TiCu/Ti-Cu-N ═┐īėų¦╝▄Ż¼XPS ūCīŹ Cu ęį Cu⁰/Cu²⁺╣▓┤µŻ¼╔·└ĒŁhŠ│ųą│ų└mßīĘ┼ Cu²⁺(0.45 μg・cm⁻²・d⁻¹)Ż¼ęųųŲ┤¾─cŚUŠ·š│ĖĮŻ¼▓ó┼c TiO₂č§╗»īėģf═¼ą╬│╔Å═║Ž▒Żūo─żŻ¼╩╣ųąĄ─Ė»╬gļŖ╬╗ūį╠ß╔²ų┴ 1.3VĪŻŠC╔ŽŻ¼═©▀^│╔ĘųįOėŗĪó╣ż╦ćģóöĄā×╗»┼c╣”─▄═┐īėģf═¼Ż¼┐╔═¼▓ĮÅŖ╗»Ōü║ŽĮų▓╚ļ╬’Ą──═╬gąį┼c╔·╬’╗ŅąįŻ¼×ķčėķLĘ■ę█ē█├³▓óĮĄĄ═Ėą╚Š’LļU╠ß╣®ą┬▓▀┬įĪŻ
2Īóį÷▓─ųŲįņ╝╝ągĻPµI╣ż╦ć┼c╠¶æ
2.1 ║╦ą─╝╝ągįŁ└Ē
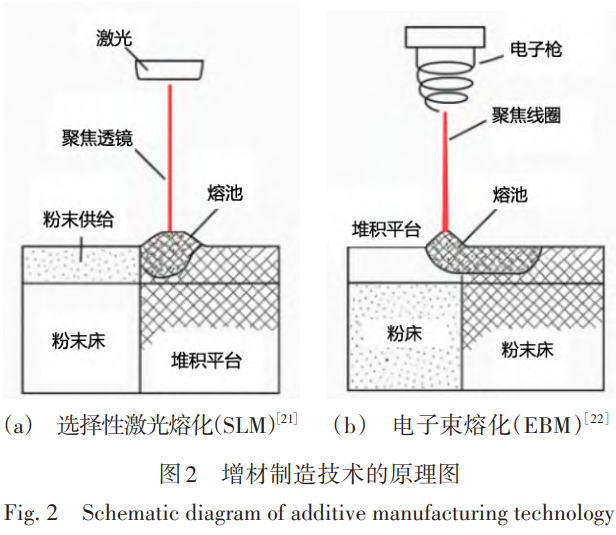
į÷▓─ųŲįņ╝╝ąg×ķŌü║ŽĮų▓╚ļ╬’Ą─╔·«a╠ß╣®┴╦ą┬═ŠÅĮŻ¼Ųõųą▀xō±ąį╝ż╣Ō╚█╗» (SLM) ║═ļŖūė╩°╚█╗» (EBM) ╩Ūā╔ĘNų„┴„Ą─Ę█─®┤▓╚█╚┌ĘĮĘ©ĪŻā╔š▀╗∙▒ŠįŁ└ĒŽÓ╦ŲŻ¼Š∙═©▀^Ė▀─▄╩°┴„ (╝ż╣Ō╗“ļŖūė╩°) į┌Įī┘Ę█─®┤▓╔Žųīė▀xō±ąį╚█╗»▓─┴ŽŻ¼īŹ¼FųīėČčĘe│╔ą═ĪŻSLM ▓╔ė├Ė▀╣”┬╩╣Ō└w╝ż╣ŌŲ„ū„×ķ─▄┴┐į┤Ż¼į┌ČĶąįÜŌ¾w▒ŻūoŽ┬╚█╗»Įī┘Ę█─®Ż¼Š▀ėą▌^Ė▀Ą─│╔ą╬Š½Č╚║═▒Ē├µ┘|┴┐ĪŻČ° EBM ät└¹ė├Ė▀─▄ļŖūė╩°ū„×ķ¤ßį┤Ż¼į┌Ė▀šµ┐šŁhŠ│ųą╚█╗»Įī┘Ę█─®Ż¼Š▀éõ╚█╗»╦┘Č╚┐ņĪóÜłėÓæ¬┴”┐žųŲ┴╝║├Ą─ā×ä▌ĪŻ
2.2 SLM ┼c EBM Ą─ī”▒╚
į÷▓─ųŲįņŽÓ▌^é„Įy£p▓─╣ż╦ć┐╔ę╗┤╬│╔ą╬Å═ļs═žōõ┼céĆ¾w╗»ų▓╚ļ╬’Ż¼’@ų°ĮĄĄ═▓─┴Žōp║─▓óē║┐s╔·«aų▄Ų┌ĪŻEBM æ{ĮĶĖ▀£žŲĮ┼_╝░ŠÅ┬²└õģsį┌─═╬gąį┼c╔·╬’╗Ņąį╔Žā×ė┌ SLMŻ¼Č° SLM ätę“Ė▀└õ╦┘½@Ą├Ė³Ė▀┴”īWÅŖČ╚ĪŻZhao Ą╚ł¾Ą└Ż¼SLM └õģs╦┘┬╩╝s 10³ ~ 10⁸Īµ・s⁻¹Ż¼╔·│╔ßśĀŅ α' ±R╩Ž¾wŻ¼┐╣└ŁÅŖČ╚ 980MPaŻ¼čė╔ņ┬╩ 8%Ż╗EBM ŅA¤ß≈700ĪµĪó└õ╦┘ 10~10²Īµ・s⁻¹Ż¼ą╬│╔ų∙ĀŅ β Š¦╝░ a ░ÕŚlŻ¼ÅŖČ╚ 920MPaŻ¼Ą½čė╔ņ┬╩ 12%ĪŻ
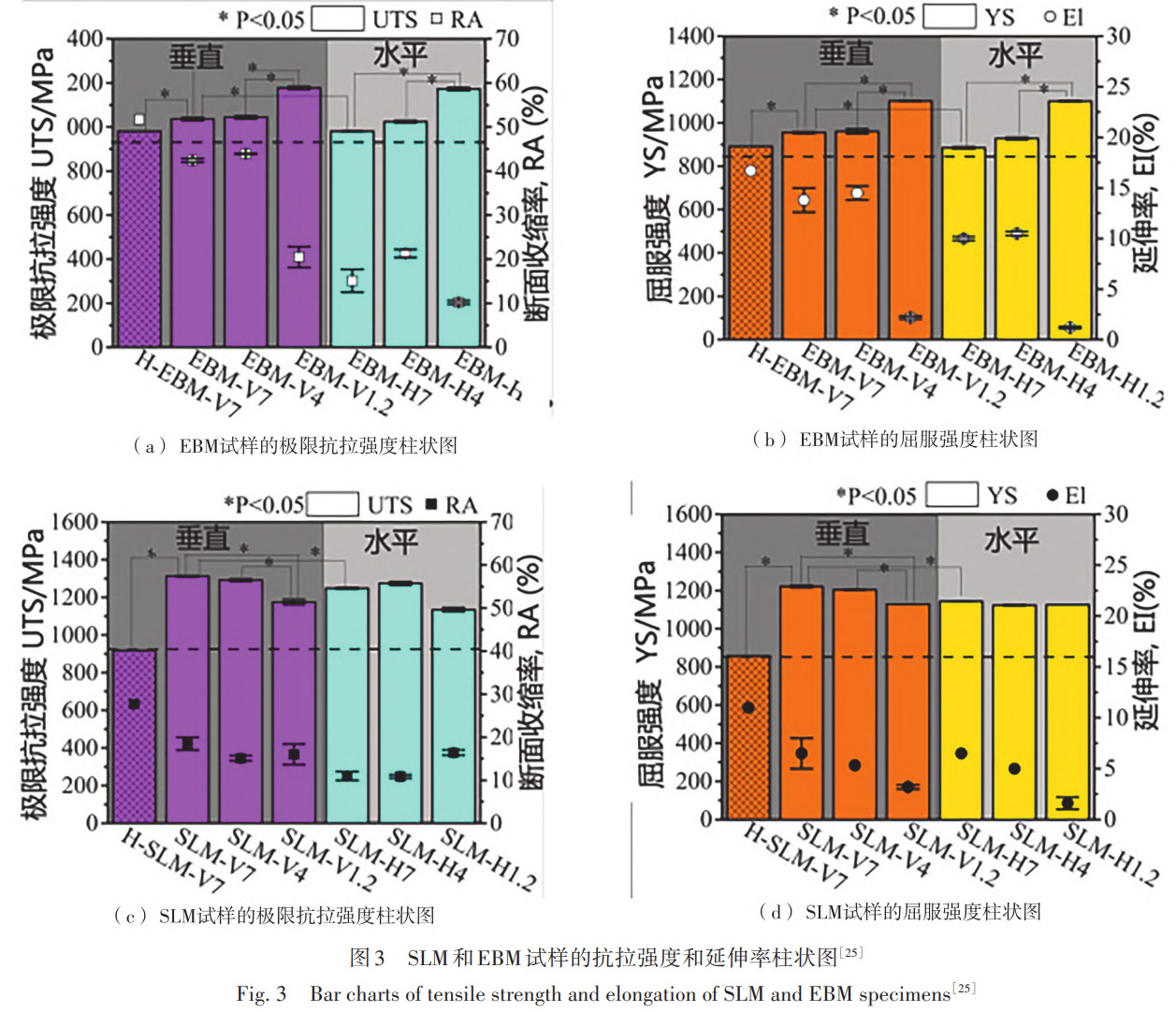
Pasang Ą╚ŽĄĮyī”▒╚┴╦ SLM ┼c EBM ųŲéõ Ti6Al-4V į┌▓╗═¼│╔ą╬ĘĮŽ“ (0°Īó45°Īó90°) Ž┬Ą─ĮM┐Ś┼c┴”īWąį─▄▓Ņ«ÉĪŻ▓╔ė├▀xō±ąį╝ż╣Ō╚█╗» (SLM) ┼cļŖūė╩°╚█╗» (EBM) ā╔ĘNĘ█┤▓╚█╚┌╣ż╦ćųŲéõįćśėŻ¼▓óĮY║Ž▒Ē├µą╬├▓ė^▓ņ (SEM)Īó’@╬óĮM┐ŚĘų╬÷Īó’@╬óė▓Č╚£yįć╝░å╬▌S└Ł╔ņīŹ“ׯ¼╚½├µįu╣└┴╦╣ż╦ć - ĮM┐Ś - ąį─▄ų«ķgĄ─ĻPŽĄĪŻčąŠ┐▒Ē├„Ż¼SLM ė╔ė┌└õģs╦┘┬╩Ė▀Ż¼ą╬│╔ęį α' ±R╩Ž¾w×ķų„Ą─╝ÜąĪĮM┐ŚŻ¼š¹¾w▒Ē¼F│÷Ė³Ė▀Ą─ė▓Č╚┼cÅŖČ╚Ą½čėąį▌^Ą═Ż╗Č° EBM į┌Ė▀£žŅA¤ßĘ█┤▓Śl╝■Ž┬│╔ą╬Ż¼½@Ą├ęįŲ¼īė α ŽÓ║═Ž╚Ū░ β Š¦Įń×ķ╠žš„Ą─ĮM┐ŚŻ¼ŲõÅŖČ╚┬įĄ═ė┌ SLMŻ¼Ą½Ė„Ž“«ÉąįŽÓī”£ž║═ĪŻÅ─│╔ą╬ĘĮŽ“┐┤Ż¼ā╔ĘN AM ▓─┴ŽŠ∙▒Ē¼F│÷├„’@Ą─ĘĮŽ“ę└┘ćąįŻ¼Ųõųą 45° ĘĮŽ“Ą─Ū³Ę■┼c┐╣└ŁÅŖČ╚Ųš▒ķūŅĖ▀ĪŻSLM ▒Ē├µĖĮų°Ą─░ļ╚█╚┌Ņw┴Ż│▀┤ń▌^ąĪ (╝s 10~40µm) ŪęĘų▓╝ŽÓī”Š∙ä“Ż¼Č° EBM ▒Ē├µ┤µį┌Ė³┤¾│▀┤ńĄ─░ļ╚█╚┌Ę█─®Ņw┴Ż (╝s 20~70µm)Ż¼ī¦ų┬Ųõ▒Ē├µ┤ų▓┌Č╚’@ų°Ė▀ė┌ SLMŻ╗ę“┤╦Ę█─®┴ŻÅĮ┼c─▄┴┐▌ö╚ļĘĮ╩Į╩Ūįņ│╔ EBM ▒Ē├µĖ³┤ų▓┌Ą─ų„ę¬įŁę“Ż¼įō▓Ņ«Éę▓┐╔─▄▀Mę╗▓Įė░ĒæŲõ┴”īWĒææ¬┼cĘ■ę█ąį─▄ĪŻMetalnikov Ą╚į┌─ŻöM¾wę║ųą£yĄ├ EBM ³c╬gļŖ╬╗ 1.1V (SLM0.8V)Ż¼Üwę“ė┌ β ŽÓ¾wĘeĘųöĄĖ▀Ūę▒Ē├µ┤ų▓┌Č╚ Ra=8.6 μmŻ╗▒M╣▄┤ų▓┌Č╚į÷┤¾Ż¼EBM č§╗»─ż═Ļš¹ąįĖ³ā×ĪŻBandekhoda Ą╚ļŖ╗»īWūĶ┐╣’@╩Š╗Ī░ļÅĮ 1.338 MΩ・cm²Ż¼╝s×ķ SLM (0.761 MΩ・cm²) ā╔▒ČŻ¼ūCīŹŲõč§╗»īėļŖūĶĖ³Ė▀ĪŻ╔·╬’╗Ņąį£yįćųąŻ¼▒Ē├µ β ŽÓšTī¦┴u╗∙┴ū╗ę╩»│┴ĘeŻ¼Ca / P=1.87Ż╗SLM ±R╩Ž¾wĮYśŗęųųŲĄV╗»Ż¼Ca/P āH 1.46ĪŻ

2.3 │╔ą═Š½Č╚┼c╚▒Ž▌┐žųŲ
▒M╣▄į÷▓─ųŲįņŠ▀éõĖ▀Č╚Äū║╬ūįė╔Č╚Ż¼│╔ą═Š½Č╚▓╗ūŃ┼c╚▒Ž▌Üł┴¶╚į╩ŪŲõ┼R┤▓▐D╗»Ą─ĻPµIŲ┐ŅiĪŻZheng Ą╚ŽĄĮy蹊┐┴╦ SLM Ōü║ŽĮČÓ┐ūų¦╝▄Ą─Š½Č╚┼c┐ūŽČ╚▒Ž▌Ż¼į┌╝ż╣Ō╣”┬╩ 200~250WĪóÆ▀├Ķ╦┘Č╚ 1000 ~ 1500 mm・s⁻¹Īóīė║±Śl╝■Ž┬Ż¼īó¾wĘe─▄┴┐├▄Č╚µiČ©ė┌ 80 ~ 100 J・mm⁻³Ż¼īŹ¼F┐ūŽČ┬╩ 65~75%Īóų┬├▄╗»┬╩ 99.2%Ż¼╬┤╚█Ņw┴Ż (PMCs) ├µĘeĘųöĄ < 2%Ż╗▒Īīė┼c▀mųąÆ▀├Ķ╦┘Č╚ģf═¼ęųųŲ╚█│ž’w×R╝░Ū“╗»Ż¼200~400µm Č©Ž“┐ūÅĮ’@ų°┤┘▀M╣ŪķL╚ļĪŻBai Ą╚ī”▒╚ EBM ┼c SLM ╚▒Ž▌ą╬│╔ÖCųŲŻ¼ųĖ│÷ EBM Ą─ 10⁻⁴Torr šµ┐š┼c 700°C ŅA¤ßĮĄĄ═č§╗»āAŽ“Ż¼└õģs╦┘┬╩ 10~102°Cs ▀hĄ═ė┌ SLM (10³ ~ 10³Īµ・s⁻¹)Ż¼ęųųŲ±R╩Ž¾wŽÓūā╬ó┴č╝yŻ╗═©▀^ļŖūė╩°ŠĆŲ½ęŲ 200µm ┼c 50µm īė║±Ż¼EBM ½@Ą├ 5~8% ęÄät▀B═©┐ūŽČŻ¼ā×ė┌ SLM Ą─ 8~12% ļSÖC╚▒Ž▌ĪŻMartinBezuidenhout Ą╚į┌ SLM ųŲéõ Ti6Al4V ųąŻ¼ęį 175~200WĪó600~800 mm・s⁻¹ ģóöĄĮM║Žīó┐ūŽČ┬╩ĮĄų┴Ż¼▓ó═¼▓ĮīŹ¼F╚f╣┼├╣╦ž┐╔┐žßīĘ┼Ż╗║¾╠Ä└Ē 20kHz │¼┬Ģš±äėÅžĄū╚ź│²Šų▓┐¤ßĘe└█ī¦ų┬Ą─ PMCsŻ¼│╔ą═Š½Č╚▀_ ±0.05mmŻ¼ØMūŃÅ═ļsČÓ┐ūŠ½£╩ųŲįņę¬Ū¾ĪŻSun Ą╚▓╔ė├ EBM Č©ųŲŌü║ŽĮūĄ¾wŻ¼ĮøļŖūė╩°─▄┴┐├▄Č╚ā×╗»║¾īėķg╬┤╚█║Ž╚▒Ž▌’@ų°£p╔┘Ż¼┐ūŽČ┬╩ĘĆČ©ė┌ 6~8%Ż¼┐ūÅĮ 350~500µmŻ╗ų▓╚ļ║¾ė░Ž±įu╣└’@╩ŠĮń├µŲź┼õŠ½Č╚ ±0.15mmŻ¼26 ų▄╣Ū - ų▓╚ļ╬’Įėė|┬╩ (BIC) ▀_ 57%Ż¼▌^é„Įyų▓╚ļ╬’ (28%) ╠ß╔²│¼▀^ę╗▒ČĪŻ
2.4 ┴”īW - ╔·╬’ąį─▄ŲĮ║ŌļyŅ}
į÷▓─ųŲįņļm┐╔Č©Ž“š{┐žŌü║ŽĮ┴”īWąį─▄Ż¼Ą½═¼▓ĮīŹ¼F┴”īW▀m┼õ┼c╣Ūš¹║Žį÷ÅŖ╚į╩Ū«öŪ░Ą─║╦ą─ļyŅ}ĪŻLuo Ą╚ęį SLM │╔ą╬ TNZTS ║ŽĮŻ¼Įø 1200°C ╣╠╚▄┤┘╩╣▒ĪÜżüåĘĆ S1 ŽÓŪ“╗»×ķ S2 ŽÓŻ¼½@Ą├Ū³Ę■ÅŖČ╚ 978MPaĪóčė╔ņ┬╩ 10.4%ĪóÅŚąį─Ż┴┐ 64.2GPa Ą─ÅŖĒgŲź┼õŻ╗Si ōĮļs▀Mę╗▓Į╠ß╔²│╔╣Ū╝Ü░¹į÷ų│╗ŅąįŻ¼ā×ė┌ Ti6Al4VŻ¼×ķČÓ╣”─▄ę╗¾w╗»įOėŗ╠ß╣®ą┬╦╝┬ĘĪŻChen Ą╚ßśī” EBM ČÓ┐ūŌüŻ¼▓╔ė├ 650°C ŅA¤ß▓óā×╗»ļpĘÕĘ█─®┴ŻÅĮŻ¼ęųųŲ “Ę█─®┤Ą’w”Ż¼╩╣┐ūŽČ▀B═©┬╩ > 95%Ż╗╦∙Ą├ų¦╝▄ÅŚąį─Ż┴┐┼c╦╔┘|╣Ūę╗ų┬Ż¼┐╣ē║ÅŖČ╚ 250MPaŻ¼¾wā╚╣ŪķL╚ļ┬╩▌^│ŻęÄ EBM ╠ß╔² 30%Ż¼į┌╣Ū┼Ķ─[┴÷ųžĮ©ųąš╣¼Fæ¬ė├Øō┴”ĪŻYin Ą╚└¹ė├ūŽ═Ō╣Ōī” 3D ┤“ėĪČÓ┐ūŌü▀Mąą▒Ē├µ╣”─▄╗»Ż¼į┌ŠS│ų 850MPa ┐╣ē║ÅŖČ╚Ū░╠ߎ┬Ż¼╠ßĖ▀▒Ē├µėH╦«ąį╝░╝Ü░¹ŽÓ╚▌ąįŻ╗═├„┴═╗╚▒ōp─Żą═’@╩ŠŻ¼ūŽ═ŌĮM╣Ū - ų▓╚ļ╬’Įėė|┬╩ė╔ 35% ╔²ų┴ 62%Ż¼ĄV╗»╣Ū▒╚└²į÷╝ė 40%Ż¼ūCīŹ▒Ē├µĖ─ąį┐╔ģf═¼ā×╗»┴”īW┼c╔·╬’ąį─▄ĪŻDuan Ą╚ęįŲÕ▒PÆ▀├Ķ▓▀┬įš{┐ž LPBF ¤ß裣hŻ¼ęųųŲ┤ÓąįŽÓ╬÷│÷Ż¼▒Ż┴¶╝{├ū α'' ±R╩Ž¾wŻ¼╩╣ 12Mo-6Zr-2Fe Ū³Ę■ÅŖČ╚▀_ 1026MPaĪóčė╔ņ┬╩ 12.7%(é„Įyå╬Ą└ <5 %)Ż¼ÅŚąį─Ż┴┐ĮĄų┴Ż╗▒Ē├µūįĮMčb TiO₂+Nb₂O₅╝{├ūč§╗»─żīó╚▄ę║ųąĖ»╬gļŖ┴„├▄Č╚ĮĄų┴ 0.1 μA・cm⁻²Ż¼│╔╣ŪĘų╗»ą¦┬╩▌^ Ti6Al4V ╠ß╔² 1.8 ▒ČŻ¼═╗ŲŲĖ▀ÅŖ β- Ōü║ŽĮ “ÅŖČ╚ - ┤Óąį - ╔·╬’ŽÓ╚▌” ╗ź│ŌŲ┐ŅiĪŻŠC╔Ž╦∙╩÷Ż¼▀@ą®čąŠ┐▒Ē├„Ż¼═©▀^ŽÓ▐Dūāš{┐žĪó┐ūĮYśŗā×╗»Īó▒Ē├µ╣”─▄╗»╝░¤ß裣hį┘įOėŗĄ╚╩ųČ╬Ż¼┐╔į┌Šų▓┐ĘČć·ā╚═╗ŲŲé„Įy “Ė▀ÅŖ - Ą═─Ż┴┐ - Ė▀╔·╬’╗Ņąį” ╚²š▀ļyęį╝µĄ├Ą─Ų┐ŅiŻ¼Ą½ę¬į┌═¼ę╗¾wŽĄųąīŹ¼F┴”īWąį─▄┼c╣Ūš¹║Ž─▄┴”╚½├µŪęķLŲ┌Ą─ŲĮ║Ō╚įąĶ▀Mę╗▓Į╠Į╦„ĪŻ
3Īóį÷▓─ųŲįņŌü║ŽĮį┌╣Ū┐ŲųąĄ─æ¬ė├
3.1 ¾yĻP╣Ø╝┘¾węį╝░¾yŠ╩╣Ūš█╣╠Č©Ą─ų▓╚ļ╬’Č©ųŲ
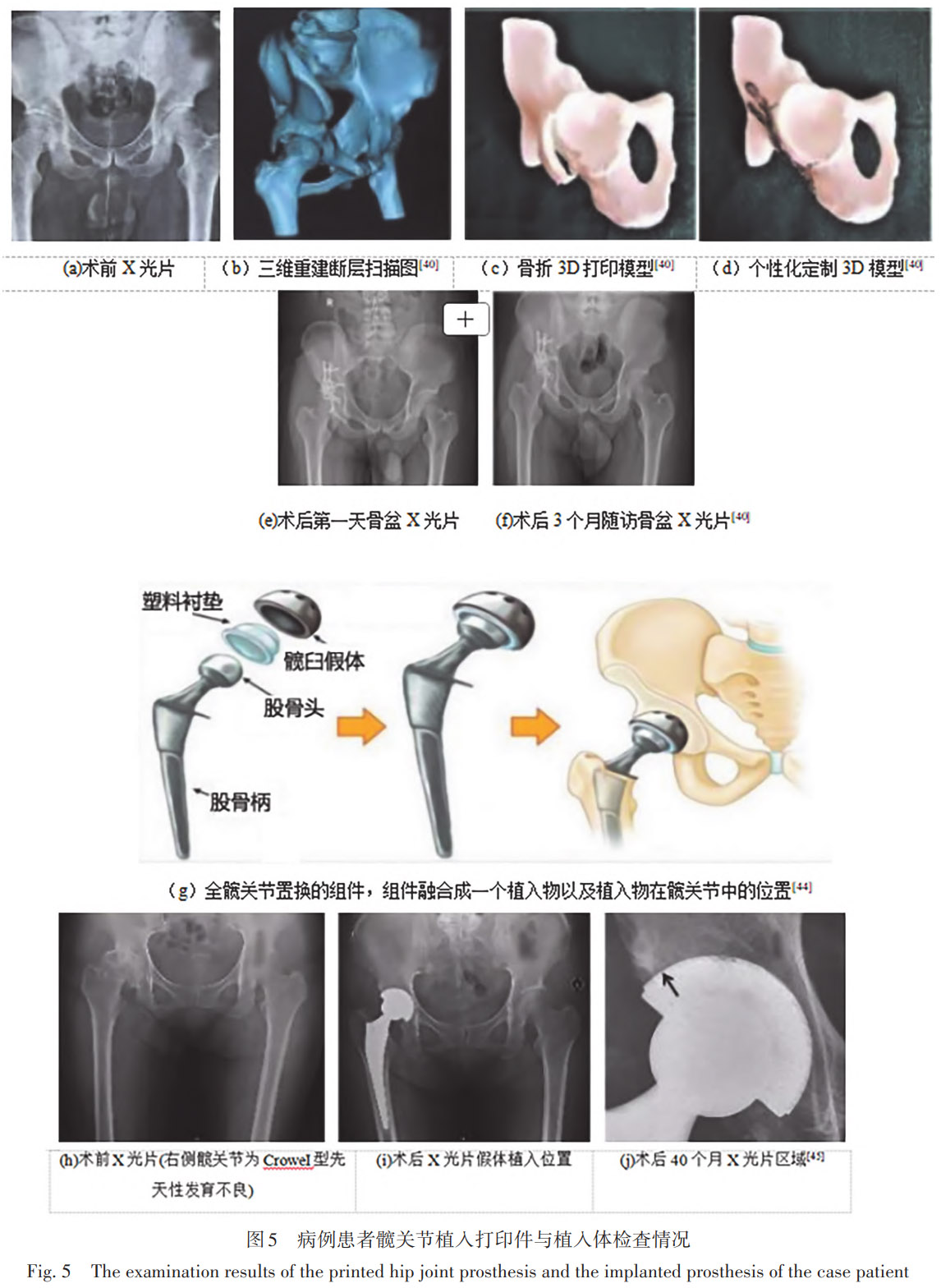
į÷▓─ųŲįņŌü║ŽĮęčė├ė┌¾yĪóŽźĻP╣Øų├ōQŻ¼┐╔ę└ō■éĆ¾wĮŌŲ╩Č©ųŲ╝┘¾wŻ¼╠ß╔²Ųź┼õČ╚▓ó╝ė╦┘ąg║¾┐ĄÅ═ĪŻTomaževičĄ╚▓╔ė├ SLM ×ķ¾yŠ╩╣Ūš█╗╝š▀Č©ųŲŌü║ŽĮĮė╣Ū░ÕŻ║ągŪ░ 3D Å═╬╗─ŻöMā×╗»░Õą╬┼cäéČ╚Ęų▓╝Ż¼ąg║¾╣Ūš█ŠĆ╬╗ęŲ▌^é„ĮyĮMĮĄĄ═ 30% (Š∙ųĄ < 1.5mm)Ż¼┐ūŽČ┬╩Š½£╩įOČ©ė┌ 15~20%Ż¼Ū³Ę■ÅŖČ╚≥850MPaŻ¼╝µŅÖÖCąĄĘĆČ©ąį┼c╣ŪķL╚ļąĶŪ¾ĪŻDrobniewski Ą╚═©▀^╗žŅÖąįķLŲ┌ļSįLĘĮĘ©Ż¼Ęų╬÷┴╦ 1999-2010 ─Ļķg 315 ├¹╗╝š▀Īó╣▓ 351 éĆ▓╔ė├Ōü║ŽĮ LCup ČÓ┐ūĖ▓īė¾yŠ╩ĮM╝■Ą─╚½¾yĻP╣Øų├ōQ (THA) ▓Ī└²Ż¼╩╣ė├ MAP įuĘųĪóVAS ╠█═┤┴┐▒Ē╝░ X ŠĆė░Ž±įu╣└Ųõų┴╔┘ 14 ─ĻĄ─┼R┤▓┼cė░Ž±īWĮY╣¹ĪŻ░l¼Fļm╚╗╩ųąg║¾╠█═┤┼c╣”─▄Š∙’@ų°Ė─╔ŲŻ¼Ą½ķLļSįLųąėą 20.5% Ą─▓Ī└²│÷¼F¾yŠ╩▒Ł╦╔äėŻ¼┐é¾w 20 ─Ļ╔·┤µ┬╩āH 73.79%Ż¼╠ß╩ŠįōŌü║ŽĮ┬▌╝y▒Łį┌ķLŲ┌ĘĆČ©ąįĘĮ├µ┤µį┌’@ų°’LļUŻ¼Ą├│÷ĮYšōŻ║L-Cup ╦∙▓╔ė├Ą─ “Ž╚Ū├ō¶į┘ą²╚ļ” Ą─╣╠Č©╬╗├µ╝╝ąg▓ó╬┤į┌ķLŲ┌▒Ē¼Fųą│╔╣”Ż¼╬┤üĒąĶę¬Ė─▀MįOėŗ┼c╩ųągĘĮ╩ĮĪŻĮY║Ž╣Ū┐ŲīŹļHæ¬ė├Ęų╬÷Ż¼░l¼FŌü║ŽĮ┬▌╝y▒ŁĮYśŗ┼c╬┤ĘŌķ]Ą─┬▌ßö┐ūęū«a╔·Š█ęꎮ─źōp╦ķą╝▓óī¦ų┬ć└ųž╣Ū╚▄ĮŌ (į┌╦╔äė▒Łųą▀_ 78%)Ż¼Ž„╚§ų▓╚ļ╬’Ą─ķLŲ┌╔·╬’╣╠Č©ąįŻ╗┬▌╝yĮYśŗį┌ķLŲ┌ųą▒Ē¼F│÷▌^Ė▀▀węŲ┬╩║═╦╔äė┬╩Ż╗┤╦═ŌŻ¼L-Cup ╩╣ė├Ą─ČÓ┐ūĄ╚ļxūėćŖ═┐Ōüīėļm┐╔┤┘▀M╣ŪĮY║ŽŻ¼Ą½ŲõķLŲ┌ĘĆČ©ąį▓╗ūŃęįĄųė∙─źōpŅw┴Ż▓Ī╝░Ę┤Å═╬óäėŻ¼Å─Č°ī¦ų┬▌^Ė▀ĘŁą▐┬╩ĪŻIkumapayi Ą╚▓╔ė├ėąŽ▐į¬Ęų╬÷ (FEA) ĘĮĘ©Ż¼į┌ ANSYS ▄ø╝■ųąĮ©┴ó┴╦╣╔╣Ū─Żą═Ż¼ī” 316L ▓╗õPõō║═Ōü║ŽĮ (Ti-6Al-4V) į┌ 2300N ▌d║╔Ž┬Ą─┴”īWąą×ķ▀Mąą┴╦─ŻöM┼c▒╚▌^ĪŻ░l¼Fį┌ČÓĘN┴”īWųĖś╦ (╚ń╝¶Ūąæ¬ūāĪóĄ╚ą¦æ¬┴”Īó┐éūāą╬Ą╚) ī”▒╚ųąŻ¼Ōü┼c▓╗õPõōĄ─Å═║Ž▓─┴Žį┌ČÓĒŚąį─▄╔Žā×ė┌å╬ę╗▓─┴ŽŻ¼ė╚Ųõį┌┐╣╝¶Ūąæ¬ūā║═┐╣ūāą╬ĘĮ├µ▒Ē¼FĖ³╝čŻ¼šf├„Å═║Ž▓─┴Ž─▄Ė³║├ŲĮ║Ōā╔š▀Ą─ā×╚▒³cŻ¼Ė³▀m║Žū„×ķ╣Ū┐Ųų▓╚ļ▓─┴ŽĪŻŌü║ŽĮį┌╣Ū┐Ųæ¬ė├ųąĄ─╚▒³cų„ę¬░³└©Ż║ÅŚąį─Ż┴┐╚įĖ▀ė┌╚╦╣ŪŻ¼ęūī¦ų┬æ¬┴”Ų┴▒╬Ż╗─═─źąį▌^▓ŅŻ¼ęū«a╔·─źōp╦ķą╝Ż╗╝¶ŪąÅŖČ╚Ą═Ż╗│╔▒Š▌^Ė▀Ż╗╝ė╣ż┼c║ĖĮė╣ż╦ćÅ═ļsŻ╗▓┐Ęų║ŽĮ (╚ń║¼ŌCĪóõX) ┐╔─▄ßīĘ┼ļxūėŻ¼ę²ŲĮM┐ŚČŠąį╗“▀^├¶Ę┤æ¬Ż╗ķLŲ┌╩╣ė├ųą┐╔─▄│÷¼FŲŻä┌öÓ┴č║═Šų▓┐Ė»╬g’LļUĪŻZhang Ą╚ęį SLM ųŲéõ¾yŠ╩║¾ų∙ČÓ┐ūŌü░ÕŻ¼┐ūÅĮ 300~500µmĪó▀B═©┬╩ > 95%Ż¼▒Ēė^─Ż┴┐≈30GPaŻ¼ĮėĮ³╦╔┘|╣ŪŻ¼’@ų°ŠÅĮŌæ¬┴”š┌ō§Ż╗12 éĆį┬ļSįL Harris įuĘų╠ßĖ▀ 18%Ż¼¤o╦╔äė╗“╣Ū╬³╩šĪŻStoffelen łFĻĀßśī”ć└ųž¾yŠ╩╚▒ōpįOėŗ│÷ SLM Ę┬╔·ČÓ┐ū╝┘¾wŻ¼┐ūŽČ┬╩ 40%ĪóąĪ┴║║± 0.3mmŻ¼ē║┐sÅŖČ╚ ≥600 MPaŻ╗─ĻļSįLīŹ¼F╣Ūąį╚┌║ŽŻ¼╠█═┤ŠÅĮŌŻ¼¤oæ¬┴”š┌ō§ąį╣ŪüG╩¦ĪŻArabnejad Ą╚╗∙ė┌╗╝š▀ CT śŗĮ©ėąŽ▐į¬─Żą═Ż¼═©▀^ČÓ│▀Č╚═žōõā×╗»┤_Č©╚½ČÓ┐ū╣╔╣Ū▒·├▄Č╚Ęų▓╝Ż¼SLM │╔ą╬║¾┐ūŽČ┬╩ 70%Īó┐ūÅĮ 500µmŻ¼ÅŚąį─Ż┴┐┐╔š{Ż╗¾w═ŌīŹ“×’@╩ŠŻ¼▌^īŹą─▒·╣Ū╬³╩š┴┐£p╔┘ 75%Ż¼Gruen ģ^ 7 ╣ŪüG╩¦┬╩ė╔ 27% ĮĄų┴ 8%Ż¼ģ^ 6 ė╔ 14% ĮĄų┴ 2%Ż¼į┌ŠS│ųÅŖČ╚Ą─═¼Ģr’@ų°Ė─╔Ų╣Ūš¹║ŽŻ¼×ķĮĄĄ═æ¬┴”Ų┴▒╬╠ß╣®ą┬ĘČ╩ĮŻ¼ć·└@╚╦╣ż¾yĻP╣Øį┌╚╦¾wā╚ķLŲ┌│ą╩▄Ė▀▌d║╔ĪóÅ═ļs╔·╬’┴”īWū„ė├╝░─”▓┴─źōpŁhŠ│▀@ę╗║╦ą─æ¬ė├ąĶŪ¾Ż¼╝╚ėąčąŠ┐Å─▓─┴Ž└Ēšōįu╩÷┼c┼R┤▓īŹ█`ā╔éĆīė├µų▓Įš╣ķ_ĪŻAherwar Ą╚┼c Singh Ą╚Å─║Ļė^▓─┴Ž¾wŽĄ│÷░lŻ¼ŽĄĮyĻU├„┴╦▓╗õPõōĪóŌü║ŽĮĪóŌÆ╗∙║ŽĮęį╝░╠š┤╔ĪóĖ▀Ęųūė╝░ŲõÅ═║Ž▓─┴Žį┌╣╔╣ŪŅ^Īó¾yŠ╩▒Ł║═╣╔╣Ū▒·Ą╚ĻPµI▓┐╬╗ųąĄ─Ę■ę█╠žąįŻ¼ųĖ│÷╚╦╣ż¾yĻP╣Ø╩¦ą¦ų„ę¬į┤ė┌─źōp╦ķą╝šT░lĄ─╔·╬’Ę┤æ¬ĪóĮī┘ļxūėßīĘ┼Īóæ¬┴”š┌ō§ą¦æ¬╝░▓─┴ŽŲŻä┌Ą╚ČÓųžę“╦žĪŻŲõųąŻ¼ŌÆ╗∙║ŽĮæ{ĮĶ▌^Ė▀Ą─ÅŖČ╚║═ŲŻä┌ąį─▄ęį╝░ę└┘ć Cr₂O₃Ōg╗»─żą╬│╔Ą─ā׫É─═─ź─═Ė»╬g─▄┴”Ż¼Ė³▀mė├ė┌│ą▌d┼c─”▓┴╝»ųąĄ─╣”─▄▓┐╬╗Ż╗Č°į┌Š█║Ž╬’¾wŽĄųąŻ¼UHMWPE ļmŠ▀éõ┴╝║├Ą─£pš┼c─═─ź╠žąįŻ¼Ą½╚į╩▄Ž▐ė┌─źōp║═╚õūāå¢Ņ}Ż¼ŽÓ▒╚ų«Ž┬Ż¼PEEK ╝░ŲõÅ═║Ž▓─┴Žį┌ĮĄĄ═─źōp┬╩║═Ė─╔Ų┴”īWŲź┼õĘĮ├µš╣¼F│÷Ė³═╗│÷Ą─ŠC║Žā×ä▌ĪŻ╔Ž╩÷蹊┐Å─└Ēšōīė├µĮę╩Š┴╦å╬ę╗▓─┴Žļyęį═¼ĢrØMūŃ╚╦╣ż¾yĻP╣Øī”┴”īWąį─▄Īó╔·╬’ŽÓ╚▌ąį┼cķLŲ┌ĘĆČ©ąįĄ─ČÓųžę¬Ū¾Ż¼ÅŖš{┴╦ČÓ▓─┴Žģf═¼įOėŗĄ─▒žę¬ąįĪŻäó│┐Ą╚īó▀@ę╗▓─┴ŽįOėŗ└Ē─Ņ┬õīŹė┌┼R┤▓īŹ█`Ż¼═©▀^ī”ś╦£╩╗» 3D ┤“ėĪČÓ┐ūŌü║ŽĮ¾yŠ╩▒Ł╚½¾yĻP╣Øų├ōQ╗╝š▀Ą─ųąŲ┌ļSįL蹊┐ūCīŹŻ¼ŅÉ╣ŪąĪ┴║ĮYśŗ┼c║Ž└Ē┐ūŽČģóöĄ─▄ē“ėąą¦┤┘▀M╣ŪķL╚ļŻ¼’@ų°Ė─╔Ųąg║¾╠█═┤┼c╣”─▄╗ųÅ═Ż¼▓óį┌ųąŲ┌ļSįLā╚īŹ¼F 100% Ą─¾yŠ╩▒Ł┤µ╗Ņ┬╩Ż¼¾w¼F│÷┴╝║├Ą─│§╩╝┼cķLŲ┌ĘĆČ©ąįĪŻŠC║ŽüĒ┐┤Ż¼Å─▓─┴Ž└ĒšōĘų╬÷ĄĮ┼R┤▓čŁūCĮY╣¹Ą─īėīėõüĻÉ▒Ē├„Ż¼ęįĖ▀ąį─▄Įī┘×ķ╣Ū╝▄ĪóĮY║ŽČÓ┐ūĮYśŗā×╗»╝░Š█║Ž╬’╗∙Å═║Ž┼c╝{├ūį÷ÅŖ▓▀┬įĄ─ģf═¼įOėŗŻ¼╩Ū╠ß╔²╚╦╣ż¾yĻP╣ØķLŲ┌Ę■ę█ąį─▄┼c┼R┤▓┐╔┐┐ąįĄ─ĻPµI░lš╣ĘĮŽ“ĪŻ
3.2 ūĄķg╚┌║ŽŲ„äōą┬įOėŗ
į÷▓─ųŲįņ×ķūĄķg╚┌║ŽŲ„╠ß╣®═žōõūįė╔Č╚Ż¼┐╔į┌▒ŻūC╔·╬’ŽÓ╚▌ąįĄ─═¼ĢrīŹ¼FÖCąĄ▀m┼õĪŻ═§Å®ĮĄ╚▓╔ė├ SLM │╔ą╬ŅiūĄ╚┌║ŽŲ„Ż¼═Ōīė┐ūŽČ┬╩ 40%Īóā╚īė 70%Ż¼Įø 900°C/150MPa ¤ßĄ╚ņoē║║¾ų┬├▄Č╚ūį 98.5% ╔²ų┴ 99.6%Ż╗ÅŚąį─Ż┴┐ 4.5GPaŻ¼Ųź┼õ╦╔┘|╣ŪŻ¼│╔ą═Š½Č╚ ±0.1mmĪŻ33 └²╗╝š▀ 2 ─ĻļSįL│┴ĮĄ┬╩āH 3%ĪŻJi Ą╚▓╔ė├ļSÖCī”ššįć“× (RCT) ī” 36 └²å╬╣ØČ╬č³ūĄ═╦ūā╗╝š▀▀Mąąī”▒╚Ż¼Ųõųą 19 └²╩╣ė├ 3D ┤“ėĪŌü║ŽĮ Ti6Al4V ūĄķg╚┌║ŽŲ„Ż¼17 └²╩╣ė├ PEEK ╚┌║ŽŲ„Ż¼═©▀^ągŪ░┼cąg║¾ VASĪóODI įuĘų╝░ X ŠĆ / CT ė░Ž±įu╣└Ųõėąą¦ąįĪó░▓╚½ąį┼cų▓╚ļ╬’ĘĆČ©ąįĪŻčąŠ┐ĮY╣¹’@╩ŠŻ¼3D ┤“ėĪŌü║ŽĮ╚┌║ŽŲ„ĮMąg║¾╠█═┤┼c╣”─▄Ė─╔Ų’@ų°Ż¼▓óŪęį┌ 3-26 éĆį┬ļSįLųą¤oę╗└²ęŲ╬╗╗“┬▌ßö╦╔äėŻ¼├„’@ā×ė┌ PEEK ĮM (17.6% ęŲ╬╗Īó5.9% ┬▌ßö╦╔äė)Ż¼ĮY╣¹▒Ē├„Ż║3D ┤“ėĪŌü║ŽĮ╚┌║ŽŲ„Š▀ėą┴╝║├╔·╬’ŽÓ╚▌ąįĪó┴”īWĘĆČ©ąį┼c┤┘▀M╣ŪķL╚ļ─▄┴”Ż¼╩Ū║¾┬Ęč³ūĄ╚┌║ŽągĄ─ėąą¦║═░▓╚½▀xō±ĪŻį┌╣Ū┐Ųæ¬ė├Ž┬Ż¼é„ĮyŌü║ŽĮĄ─ąį─▄▓╗ūŃŻ║ė╔ė┌ÅŚąį─Ż┴┐├„’@Ė▀ė┌ūĄ¾w╣ŪĮM┐ŚŻ¼Ģ■«a╔·æ¬┴”š┌ō§Ż¼ī¦ų┬╚┌║ŽŲ„│┴ĮĄ’LļUį÷╝ėŻ¼▀@ę╗³c╩ŪķLŲ┌╩╣ė├Įī┘╚┌║ŽŲ„Ą─╔·╬’┴”īW╚▒Ž▌Ż╗┤╦═ŌŻ¼Įī┘į┌é„Įy╝ė╣żĘĮ╩ĮŽ┬▒Ē├µ╣Ō╗¼Ż¼▒Ē├µ╣ŪĮY║Ž─▄┴”▓╗ūŃŻ¼┐╔─▄ė░Ēæ╣Ū╚┌║ŽĪŻę“┤╦ÅŖš{═©▀^ 3D ┤“ėĪśŗĮ©Ė▀▀_ 80% ┐ūŽČ┬╩ĪóŅÉ╦╔┘|╣ŪĮYśŗ╝░┤ų▓┌▒Ē├µŻ¼š²╩Ū×ķ┐╦Ę■é„ĮyŌü║ŽĮį┌╣Ū┐Ųæ¬ė├ųą “Ė▀─Ż┴┐ī¦ų┬│┴ĮĄ” ║═ “▒Ē├µ╣Ūš¹║Ž▓╗ūŃ” Ą─╚▒³cŻ¼▓ó╠ß╔²ų▓╚ļ╬’╔·╬’īWąį─▄ĪŻShuai Ą╚╗∙ė┌ėąŽ▐į¬Ęų╬÷ (FEA) ĘĮĘ©Ż¼śŗĮ©┴╦Ę¹║ŽšµīŹĮŌŲ╩ĮYśŗĄ─ L4L5 č³ūĄ║¾┬ĘūĄķg╚┌║Ž (PLIF) ─Żą═Ż¼ī”▒╚įu╣└┴╦ 3D ┤“ėĪČÓ┐ū│¼Ą═ÅŚąį─Ż┴┐ Ti-24Nb-4Zr-8Sn (Ti2448) ╚┌║ŽŲ„ĪóČÓ┐ū Ti-6Al-4V (Ti64) ╚┌║ŽŲ„┼cé„Įy PEEK ╚┌║ŽŲ„į┌ČÓĘN╔·└Ē╣żørŽ┬Ą─╔·╬’┴”īWąą×ķĪŻčąŠ┐═©▀^▒╚▌^ūĄķg╗ŅäėČ╚ (ROM)ĪóūĄ╣ŁĖ∙ßö░¶ŽĄĮyæ¬┴”Īó╚┌║ŽŲ„ - ĮK░ÕĮń├µæ¬┴”╝░Įń├µ╬óäėĄ╚ĻPµIųĖś╦Ż¼░l¼Fā╔ĘNČÓ┐ūŌü║ŽĮ╚┌║ŽŲ„š¹¾wĘĆČ©ąįā×ė┌ PEEKŻ¼ŲõųąĄ═ÅŚąį─Ż┴┐ Ti2448 ╚┌║ŽŲ„į┌ĮĄĄ═ĮK░ÕĮń├µæ¬┴”ĪóĖ─╔Ųæ¬┴”Ęų▓╝╝░£p╔┘│┴ĮĄ’LļUĘĮ├µ▒Ē¼FūŅ×ķ═╗│÷Ż¼Ųõ┴”īWĒææ¬Ė³ĮėĮ³╚╦¾w╣ŪĮM┐ŚŻ¼ėą└¹ė┌ķLŲ┌╣Ūš¹║ŽĪŻSun Ą╚ć·└@ŅiūĄŪ░┬ĘūĄķg╚┌║Žąg (ACDF)Ż¼▓╔ė├ėąŽ▐į¬Ęų╬÷ (FEA) ĘĮĘ©śŗĮ©┴╦š²│ŻŅiūĄ─Żą═Ż¼Ęųäeų▓╚ļ ZK60 µV║ŽĮ╚┌║ŽŲ„ĪóTi-6Al-4V Ōü║ŽĮ╚┌║ŽŲ„Ą─╩ųąg─Żą═Ż¼▓óį┌Ū³Ū·Īó╔ņš╣Īóé╚ÅØ║═▌SŽ“ą²▐DĄ╚╣żørŽ┬ŽĄĮy▒╚▌^┴╦╗ŅäėČ╚ (ROM)Īó╚┌║ŽŲ„ūāą╬Īó╚┌║ŽŲ„╝░╣ŪęŲų▓╬’æ¬┴”ęį╝░ĮK░Õ - ╚┌║ŽŲ„Įń├µæ¬┴”Ż╗į┌┤╦╗∙ĄA╔ŽŻ¼▀Mę╗▓Į╗∙ė┌╩▄┴”╠žš„ī” ZK60 ╚┌║ŽŲ„▀MąąŠ¦Ė±═žōõā×╗»įOėŗ▓ó▀Mąą┴”īW“×ūCĪŻĮY╣¹▒Ē├„Ż¼┼cŌü║ŽĮ╚┌║ŽŲ„ŽÓ▒╚Ż¼ZK60 ╚┌║ŽŲ„┐╔į┌▒Ż│ųŅiūĄš¹¾wĘĆČ©ąįĄ─═¼Ģr’@ų°ĮĄĄ═╚┌║ŽŲ„╝░ĮK░ÕĮń├µæ¬┴”Ż¼£p╚§æ¬┴”š┌ō§ą¦æ¬Ż¼▓ó╠ßĖ▀╣ŪęŲų▓╬’╦∙╩▄Ą─┴”īW┤╠╝ż (ŲĮŠ∙╠ßĖ▀╝s 27.7%)Ż¼Å─Č°Ė³ėą└¹ė┌╣Ū╚┌║ŽŻ╗Č°ĮøŠ¦Ė±═žōõā×╗»║¾Ą─ČÓ┐ū ZK60 ╚┌║ŽŲ„į┌▀Mę╗▓ĮĮĄĄ═ĮYśŗäéČ╚║═Įń├µæ¬┴”Ą─═¼ĢrŻ¼▒Ē¼F│÷Ė³āץ─╔·╬’┴”īWąį─▄ĪŻū„š▀ō■┤╦šJ×ķŻ¼ZK60 ╝░ŲõŠ¦Ė±ā×╗»ĮYśŗį┌ĮĄĄ═│┴ĮĄ’LļUĪó┤┘▀M╣Ū╚┌║ŽĘĮ├µŠ▀ėą├„’@ā×ä▌Ż¼╩Ūę╗ĘNŠ▀ėąæ¬ė├Øō┴”Ą─ŅiūĄ╚┌║ŽŲ„įOėŗĘĮ░ĖĪŻMcGilvray Ą╚═©▀^▓╔ė├äė╬’─Żą═īŹ“×ĘĮĘ©Ż¼į┌Šdč“č³ūĄ╚┌║Ž─Żą═ųąų▒Įė▒╚▌^┴╦ 3D ┤“ėĪČÓ┐ūŌü║ŽĮ (PTA)ĪóŠ█├č├č═¬ (PEEK) ęį╝░Ą╚ļxūėćŖ═┐ČÓ┐ūŌü═┐īė PEEK (PSP) ╚²ĘNūĄķg╚┌║ŽŲ„Ą─ąį─▄ĪŻčąŠ┐═©▀^╔·╬’┴”īW£yįćĪó╬ó CT Æ▀├Ķ║═ĮM┐Śą╬æBėŗ┴┐īWĘų╬÷Ż¼░l¼F PTA į┌╣ŪķL╚ļĪó╔·╬’┴”īWĘĆČ©ąį (╚ńĮĄĄ═▀\äėĘČć·Īó╠ßĖ▀äéČ╚) ęį╝░╣Ūš¹║ŽĘĮ├µŠ∙’@ų°ā×ė┌ PEEK ║═ PSPŻ¼ė╚Ųõį┌ 16 ų▄Ģr▒Ē¼F│÷Ė³ÅŖĄ─╣Ūš¹║Ž─▄┴”║═ĮYśŗĘĆČ©ąįĪŻMakino Ą╚═©▀^ę╗ĒŚ┼R┤▓▓Ī└²ŽĄ┴ąčąŠ┐Ż¼▒╚▌^┴╦╩╣ė├Ōü═┐īėŠ█├č├č═¬ (TCP) ╗\┼c╚²ŠSČÓ┐ūŌü║ŽĮ (PTA) ╗\▀Mąą║¾┬Ęč³ūĄūĄķg╚┌║Žąg (PLIF) ║¾Č╠Ų┌ (≤1 ─Ļ) Ą─ė░Ž±īW┼c┼R┤▓ĮYŠųĪŻčąŠ┐ĘĮĘ©░³└©ī” 63 └²╗╝š▀▀Mąą╗žŅÖąįĘų╬÷Ż¼įu╣└╚┌║ŽĀŅæBĪóĮK░Õ─ę─[ą╬│╔Īó╚┌║ŽŲ„│┴ĮĄ╝░╗╝š▀ł¾ĖµĄ─╔·╗Ņ┘|┴┐ (╗∙ė┌ JOABPEQ 墊Ē)ĪŻĮYšō’@╩ŠŻ¼ā╔ĮM╗╝š▀į┌ąg║¾ 1 ─ĻĄ─╚┌║Ž┬╩┼c╔·╗Ņ┘|┴┐Ė─╔ŲĘĮ├µ¤o’@ų°▓Ņ«ÉŻ¼Ą½ PTA ╗\ĮMį┌ąg║¾ 6 éĆį┬Ą─ĮK░Õ─ę─[ą╬│╔║═╚┌║ŽŲ„│┴ĮĄ│╠Č╚’@ų°Ą═ė┌ TCP ╗\ĮMŻ¼▒Ē├„ PTA ╗\į┌įńŲ┌╣╠Č©║═ęųųŲŠų▓┐╣Ū╬³╩šĘĮ├µĖ³Š▀ā×ä▌ĪŻ╬─ųąųĖ│÷Ōü║ŽĮū„×ķ╚┌║ŽŲ„▓─┴ŽĄ─╚▒³cų„ę¬░³└©Ż║ŲõäéČ╚Ė▀ė┌╣Ū„└Ż¼┐╔─▄ī¦ų┬æ¬┴”Ų┴▒╬ą¦æ¬Ż¼▀MČ°ė░Ēæ╣Ūė·║Ž▓óį÷╝ė╚┌║ŽŲ„│┴ĮĄ’LļUŻ╗┤╦═ŌŻ¼Ōü═┐īėį┌ų▓╚ļ▀^│╠ųą┐╔─▄░l╔·äāļxŻ¼«a╔·Ą──źą╝┐╔─▄ę²░lčū░YĘ┤æ¬Ż¼┤┘▀MĮK░Õ─ę─[ą╬│╔┼cöU╔óĪŻDonaldson Ą╚Ęų╬÷┴╦ 50 └²╩╣ė├ 3D ┤“ėĪČÓ┐ūŌü║ŽĮ (3D Ti) ╚┌║ŽŲ„ąąč³ūĄŪ░┬Ę╗“é╚┬ĘūĄķg╚┌║Ž╩ųągĄ─╗╝š▀┘Y┴Ž (╣▓ 66 éĆ╩ųąg╣ØČ╬)ĪŻę└ō■ Gruskay ś╦£╩įu╣└╚┌║ŽŪķørŻ¼▓ó░┤ Marchi Ęų╝ē┼ąöÓ╚┌║ŽŲ„│┴ĮĄĪŻĮYšō▒Ē├„Ż¼3D ┤“ėĪŌü║ŽĮ╚┌║ŽŲ„į┌č³ūĄŪ░┬Ę┼cé╚┬Ę╚┌║Žągųą┐é¾w│┴ĮĄ┬╩×ķ 3.03%Ż¼į┘╩ųąg┬╩×ķ 1.5%Ż¼’@ų°Ą═ė┌╬─½Ił¾Ą└Ą─é„Įy PEEK ╗“īŹą─Ōü║ŽĮ╚┌║ŽŲ„Ą─öĄō■ĪŻ

3.3 Ž┬ŅM╣ŪųžĮ©
į÷▓─ųŲįņ┐╔Š½£╩Ųź┼õŽ┬ŅM╣ŪÅ═ļsĮŌŲ╩Ż¼īŹ¼FŌü║ŽĮų▓╚ļ╬’éĆ¾w╗»ą▐Å═ĪŻXue Ą╚ęįėąŽ▐į¬ā×╗» 3D ┤“ėĪŌü░Õ (16mm×2.8mmŻ¼10 ├Č┬▌ßö)Ż¼æ¬┴”Ęų▓╝Š∙ä“Ūę▒▄├ŌŲ┴▒╬Ż╗78 Üq│╔ėį╝Ü░¹┴÷Å═░l╗╝š▀ąg║¾ CT ’@╩Š┘N║Ž┴╝║├Ż¼ę¦║Ž╣”─▄╗ųÅ═Ż¼ķLŲ┌ļSįL¤o░ÕöÓ┴č╗“┬▌ßö╦╔äėĪŻZhao Ą╚▓╔ė├ SLM │╔ą╬ŠWĀŅŽ┬ŅM╝┘¾wŻ¼ANSYS ŲŻä┌Ęų╬÷▒Ē├„Ż¼0.5mm ĮzÅĮ┐╔│ą╩▄ 4 ┤╬裣hŻ¼ĮzÅĮ│¼▀^ 6 ×10⁵┤╬╚į═Ļš¹Ż╗▒╚Ė±╚«░ļé╚╚▒ōp─Żą═ųą╝┘¾w¤oąĶ╦▄ą╬╝┤Š½£╩┘N║ŽŻ¼6 éĆį┬ CT ’@╩ŠŽ┬ŅMą╬æB┼c’DŽ┬ŅMĻP╣ØĘĆČ©Ż¼¤oĖ╬─IČŠąįĪŻShi Ą╚╚╦═©▀^ėąŽ▐į¬Ęų╬÷ (FEA)Īóņo┴”īWĘų╬÷ĪóĮŽÓĮM┐Ś┼cė▓Č╚£yįć (358±14HV)ĪóöÓ┐┌ SEM Ęų╬÷Ą╚ČÓŠSĘĮĘ©Ż¼ī”ę╗└²į┌¾wā╚╩╣ė├ 34 éĆį┬║¾░l╔·öÓ┴čĄ─éĆ¾w╗» Ti-6Al-4V Ž┬ŅMųžĮ©░Õ▀MąąŽĄĮy╩¦ą¦čąŠ┐ĪŻFEA ’@╩Šų▓╚ļ░Õį┌ŠūĮ└Ģr│ą╩▄Ą─ūŅ┤¾└Łæ¬┴”╝s×ķ 392.6MPaŻ¼ĮėĮ³▓─┴Ž 510MPa Ą─ŲŻä┌ÅŖČ╚Ż¼░▓╚½ŽĄöĄāH 1.3Ż¼Ūęæ¬┴”Ė▀Č╚╝»ųąė┌ S5 ┬▌┐ūĖĮĮ³Ż¼▀@╩ŪöÓ┴čūŅ│§░l╔·Ą─▓┐╬╗ĪŻĮŽÓĘų╬÷▒Ē├„▓─┴Žų┬├▄Č╚▀_ 99.8±0.05%Ż¼Ą½╚į┤µį┌╬ó┐ū╝░ α/α'β ĮM┐ŚŻ¼╩╣Šų▓┐│╔×ķŲŻä┌┴č╝y├╚╔·³cŻ╗öÓ┐┌ SEM ’@╩ŠĄõą═Ą─ŲŻä┌Śl╝yĪóĮŌ└Ē┼_ļA║═ĒgĖCŻ¼ūCīŹŲõ×ķĖ▀ų▄ŲŻä┌ų„ī¦Ą─╗ņ║Ž┤Ó - ĒgöÓ┴č─Ż╩ĮĪŻ┤╦═ŌŻ¼┴č╝yā╚▓┐Öz£yĄĮ Ca/P/O │┴Ęe║═╔·╬’ę║šTī¦Ą─Üõ┤Ó█EŽ¾Ż¼▀Mę╗▓Į╝ė╦┘┴č╝yöUš╣ĪŻ═¼ĢrųĖ│÷Ż¼į┌╣Ū┐Ųæ¬ė├ųą Ti6Al-4V Ą─ų„ę¬╚▒³cį┌ė┌Ż║ŲõÅŚąį─Ż┴┐ (113.8GPa) ▀hĖ▀ė┌Ųż┘|╣Ū (13.7GPa)Ż¼ęūī¦ų┬æ¬┴”Ų┴▒╬Ż╗ŲŻä┌ÅŖČ╚ėąŽ▐Ż¼į┌ķLŲ┌Å═ļsę¦║Ž┴”ū„ė├Ž┬ęū░l╔·ŲŻä┌┴č╝yŻ╗┤╦═Ō SLM ųŲéõĄ─ų▓╚ļ╬’▒Ē├µ╚į┐╔─▄┤µį┌╬ó┐ūĪóÄū║╬▒Ī╚§ģ^╝░æ¬┴”╝»ųąŻ¼Š∙’@ų°ĮĄĄ═į┌¾wā╚Ę■ę█ē█├³ĪŻDündar Ą╚╚╦▓╔ė├ėąŽ▐į¬Ęų╬÷ĘĮĘ©Ż¼ī”▒╚┴╦Ōü║ŽĮ╣╠Č©░Õ┼cµćŌüą╬ĀŅėøæøßöų╬»¤Ž┬ŅM╣Ū╣Ūš█Ą─╔·╬’┴”īWąį─▄ĪŻ░l¼Fį┌ 200N ę¦║Ž┴”ū„ė├Ž┬Ż¼NiTi ą╬ĀŅėøæøßö (ė╚Ųõ╩Ū╚²ßöŪęųąčļßö│╩ + 30° ĮŪĄ─ūŅ╝č┼õų├) «a╔·Ą─ūŅ┤¾æ¬┴” (67.16MPa) ’@ų°Ą═ė┌Ōü░Õ (å╬░Õ 194.62MPaŻ¼ļp░Õ 157.47MPa)Ż¼Ūęā╔š▀«a╔·Ą─╣ŪēK╬╗ęŲŠ∙╠Äė┌└¹ė┌╣Ūė·║ŽĄ─╬óäėĘČć· (0.1–0.8mm) ā╚Ż¼▒Ē├„ NiTi ßöį┌╠ß╣®ūŃē“ĘĆČ©ąįĄ─═¼ĢrŻ¼─▄Ė³āץžĘų╔óæ¬┴”Ż¼╩ŪŌü░ÕĄ─ę╗ĘNėąŪ░Š░Ą─╠µ┤·ĘĮ░ĖĪŻŪęųĖ│÷Ōü║ŽĮų▓╚ļ╬’ų„ę¬┤µį┌ęįŽ┬╚▒³cŻ║ŲõäéąįĮYśŗ╝░┬▌ßö┐ūęūī¦ų┬æ¬┴”╝»ųą║═æ¬┴”Ų┴▒╬Ż¼┐╔─▄ę²░l╣Ū╬³╩šŻ╗┼R┤▓▓ó░l░Y▌^ČÓŻ¼░³└©ų▓╚ļ╬’┐╔ė|╝░Īó└õ├¶ĖąŻ¼Č■┤╬╩ųągęŲ│²┬╩Ė▀▀_ 10%–23.4%Ż¼Ėą╚Š┬╩╝s 3%–23%Ż╗ķLŲ┌╔·╬’ŽÓ╚▌ąįĘĮ├µŻ¼┤µį┌Įī┘ļxūėßīĘ┼ĪóØōį┌▀^├¶Ę┤æ¬ęį╝░į┌╠žČ©ŁhŠ│Ž┬Ė»╬gĄ─’LļUĪŻAlmudarris Ą╚ī” 30 └²Ž┬ŅM╚▒ōpąą╝ż╣ŌĘ█─®┤▓╚█╚┌Č©ųŲ Ti6Al4V ų▓╚ļ▓ó┬ō║Ž▄øĮM┐ŚęŲų▓Ż¼12 éĆį┬┤µ╗Ņ┬╩ 96.7%Ż¼ŠūĮ└ą¦┬╩╠ßĖ▀ 40%Ż¼šZčįŪÕ╬·Č╚į÷╝ė 30%Ż¼85% ╗╝š▀├└īWįuār “ā׹єŻ¼āH 2 └²▌pČ╚Ėą╚ŠĪó1 └²╦╔äėĪŻHijazi Ą╚ęį SLM śŗĮ©å╬╬╗Š¦░¹ 1mmĪóų¦ų∙ 350~450µm Ą─║åå╬┴óĘĮČÓ┐ū Ti6Al4VŻ¼ÅŚąį─Ż┴┐╝s 20~30GPaŻ¼┼cŲż┘|╣ŪŲź┼õŻ╗ŲŻä┌─ŻöMė┌ 50~100N ŠūĮ└▌d║╔Ž┬ē█├³ 4~119 ─ĻŻ¼ų▓╚ļ║¾ŲŻä┌ÅŖČ╚ĘŁ▒ČĪŻ╠▌Č╚ĮYśŗ╝µŅÖ┴”īW▀m┼õ┼c╣Ūš¹║ŽŻ¼×ķŽ┬ŅM╣Ū╚▒ōp╠ß╣®éĆ¾w╗»ĮŌøQĘĮ░ĖĪŻ
4 ĮYšō┼cš╣═¹
Ōü║ŽĮęįŲõĖ▀▒╚ÅŖČ╚Īóā׫É╔·╬’ŽÓ╚▌ąį┼cūįŌg╗»─═╬g─▄┴”Ż¼│╔×ķ═╗ŲŲé„ĮyĮī┘ “┴”īW╩¦┼õ - ╔·╬’ČĶąį” Ų┐ŅiĄ─└ĒŽļ╣Ū┐Ųų▓╚ļ▓─┴ŽĪŻ▀xģ^╝ż╣Ō╚█╗» (SLM) ┼cļŖūė╩°╚█╗» (EBM) ═©▀^ųīė└█╝ė▓▀┬įŻ¼īŹ¼FĮŌŲ╩╝ēÄū║╬Å═¼F┼c┐ūŽČ╠žš„Š½┤_┐žųŲŻ¼Ęųäeį┌│╔ą╬Š½Č╚╝░ĮM┐ŚėH║═ĘĮŽ“ą╬│╔╗źčaĪŻ┼R┤▓ūCō■ęčūCīŹ 3D ┤“ėĪŌü║ŽĮį┌¾yĪó╝╣ų∙┼cŅM├µą▐Å═ųąĄ─░▓╚½ąįĪó┴”īW▀m┼õąį┼c╣”─▄ųžĮ©ą¦─▄ĪŻ╬┤üĒ蹊┐ąĶŠ█Į╣ė┌│╔Ęų - ĮYśŗģf═¼įOėŗŻ¼śŗĮ©─Ż┴┐╠▌Č╚ČÓ┐ū┐“╝▄▓ó±Ņ║Ž╔·╬’╗Ņąį═┐īėŻ¼ęį═¼▓ĮĮĄĄ═æ¬┴”Ų┴▒╬Īó┤┘▀M╣Ūš¹║ŽŻ╗┴Ēę╗ĘĮ├µŻ¼ąĶ╣ź┐╦į÷▓─▀^│╠┐ūČ┤Īó╬┤╚█Ņw┴Ż┼c▒Ē├µ┤ų▓┌Č╚╚▒Ž▌Ż¼═©▀^ČÓģóöĄ±Ņ║Žā×╗»┼c║¾╠Ä└Ēķ]Łh┐žųŲŻ¼▒ŻšŽÅ═ļsų▓╚ļ╬’į┌ķLŲ┌╔·└Ē▌d║╔Ž┬Ą─ŲŻä┌┐╔┐┐ąį┼c╗»īWĘĆČ©ąįĪŻ═ŲäėéĆąį╗»Ōü║ŽĮų▓╚ļ╬’Ž“ś╦£╩╗»ĪóęÄ─Ż╗»č▌▀MŻ¼╝»│╔╚╦╣żųŪ─▄╦ŃĘ©Īóė░Ž±─µŽ“Į©─Ż┼cĘ┬╔·═žōõā×╗»Ż¼Į©┴óĖ▀▒ŻšµĪó┐ņĒææ¬Ą─┼R┤▓Č©ųŲŲĮ┼_Ż¼īó╩ŪīŹ¼FŠ½£╩╣Ū┐Ųą▐Å═Ą─ųžę¬ĘĮŽ“ĪŻ
ģó┐╝╬─½I
[1] └ŅåóśsŻ¼└Ņ╬─▓®Ż¼┼Ż│■║ŁŻ¼Ą╚ĪŻ╣Ū┐Ųė├Ōü║ŽĮ▒Ē├µĖ─ąį╝╝ąg┼c╔·╬’ŽÓ╚▌ąį蹊┐▀Mš╣ [J]. Ōü╣żśIŻ¼2021,38 (5):41-48. Li Qirong, Li Wenbo, Niu Chuhan, et al. Research Progress on Surface Modification Technology and Biocompatibility of Titanium Alloy for Orthopedics [J]. 2021, 38 (5): 41-48.
[2] ╦╬▓®Ż¼░▓├„ėŅŻ¼═§╝tĻ¢Ż¼Ą╚ĪŻ╣╠╚▄└õģsĘĮ╩Įī”ą┬ą═Ė▀ÅŖĮ³ β Ōü║ŽĮ Ti-5321 ╬óė^ĮM┐Ś╝░┴”īWąį─▄Ą─ė░Ēæ [J]. ┴─│Ū┤¾īWīWł¾ (ūį╚╗┐ŲīW░µ), 2024, 37 (3): 53-61. Song Bo, An Mingyu, Wang Hongyang, Wang Yisen, Zhen Jinming. Effect of Cooling Method After Solution on Microstructure and Mechanical Properties of New Near-β Ti Alloy Ti-5321 [J]. Journal of Liaocheng University (Natural Science Edition), 2024, 37 (3): 53-61.
[3] ╦╬▓®Ż¼░▓├„ėŅŻ¼─▀┐ĪĮ▄Ż¼Ą╚ĪŻĮ■┼▌£žČ╚║═Ģrķgī”║Żč¾ĮYśŗŌü║ŽĮ─═╬gąį─▄Ą─ė░Ēæ [J]. ┴─│Ū┤¾īWīWł¾ (ūį╚╗┐ŲīW░µ),2024,37 (6):62-70. Song Bo, An Mingyu, Ni Junjie, et al. Effect of Immersing Temperature and Duration on Corrosion Resistance of Ti Alloy in Marine Field [J], Journal of Liaocheng University (Natural Science Edition), 2024, 37 (6): 62-70.
[4] ÅłįŲ²łŻ¼ČŁ÷╬ņ═Ż¼ĄįĶ„Ś¦Ż¼Ą╚. Er₂O₃╬ó┴ŻōĮļsī” TC4 Ōü║ŽĮ╬ó╗Īč§╗»═┐īėĮM┐Ś║═─═─źąįĄ─ė░Ēæ [J]. ŽĪėąĮī┘Ż¼2024,48 (8):1120-1131. Zhang Yunlong, Dong Xinyan, Zhai Ziyu, et al. Microstructure and Wear Resistance of MAO Coatings of TC4 Alloy with Different Er₂O₃ Doping Amounts [J]. 2024, 48 (8):1120-1131.
[5] Č┼ųęą±Ż¼ę³┘O▒“Ż¼╦╬▓®Ż¼Ą╚ĪŻ╬ó╗Īč§╗»ųŲéõßtė├Ōü║ŽĮ╔·╬’Å═║Ž═┐īė蹊┐▀Mš╣ [J]. ┴─│Ū┤¾īWīWł¾ (ūį╚╗┐ŲīW░µ), 2025, 38 (3): 404-410. Du Zhongxu, Yin Yibin, Song Bo, NI Junjie, DI Heyang, LIU Zhiwen. Research progress of biocomposite coatings on medical titanium alloy prepared by micro-arc oxidation [J]. Journal of Liaocheng University (Natural Science Edition), 2025, 38 (3): 404-410.
[6] Ampadi Ramachandran, Remya, et al. Artificial intelligence and machine learning as a viable solution for hip implant failure diagnosis-Review of literature and in vitro case study [J]. Medical & Biological Engineering & Computing61.6 (2023): 1239-1255.
[7] Wu, Puzhen, et al. Personalization and Precision: Innovative Applications and Future Challenges of Additive Manufacturing in Orthopedic Implants [J]. Journal of Orthopaedic Research, 2025: 1-17.
[8] Lal, Hitesh, and Mohit Kumar Patralekh. 3D printing and its applications in orthopaedic trauma: a technological marvel [J]. Journal of clinical orthopaedics and trauma,2018,9 (3): 260-268.
[9] Ozan S, Lin J, Li Y, et al. Development of Ti–Nb–Zr alloys with high elastic admissible strain for temporary orthopedic devices [J]. Acta biomaterialia, 2015, 20: 176-187.
[10] Daniel Devaraj L, Srinivasan V. Evaluation of Microhardness, Compression, and Flexural Strength for Gyroid Ti-6Al-4V with Different Porosities Fabricated by Direct Metal Laser Sintering Process for Orthopedic Application [J]. Journal of Materials Engineering and Performance, 2025:1-13.
[11] Murr L E, Amato K N, Li S J, et al. Microstructure and mechanical properties of open-cellular biomaterials prototypes for total knee replacement implants fabricated by electron beam melting [J]. Journal of the mechanical behavior of biomedical materials, 2011, 4 (7): 1396-1411.
[12] McMahon, Rebecca E, et al. A comparative study of the cytotoxicity and corrosion resistance of nickel–titanium and titanium – niobium shape memory alloys [J]. Acta biomaterialia, 2012,8 (7): 2863-2870.
[13] Liu Q, Zhang Y, Chen W, et al. Bioactive and fatigue-resistant Ti–Ta alloy by additive manufacturing for orthopedic applications [J]. Smart Materials in Manufacturing, 2025, (3): 100086.
[14] Guo Y, Wu J, Xie K, et al. Study of bone regeneration and osteointegration effect of a novel selective lasermelted titanium-tantalum-niobium-zirconium alloy scaffold [J]. ACS Biomaterials Science & Engineering, 2019, 5 (12): 6463-6473.
[15] Jing Z, Yuan W, Wang J, et al. Simvastatin/hydrogel-loaded 3D-printed titanium alloy scaffolds suppress osteosarcoma via TF/NOX2-associated ferroptosis while repairing bone defects [J]. Bioactive materials, 2024, 33: 223-241.
[16] Xue Pengfei, et al. Superelasticity, corrosion resistance and biocompatibility of the Ti – 19Zr – 10Nb – 1Fe alloy [J]. Materials Science and Engineering: C, 2015 (50): 179-186.
[17] Li J, Zhong H, Cao B, et al. Comparative Study of 3D-Printed Porous Titanium Alloy with Rod Designs of Three Different Geometric Structures for Orthopaedic Implantation [J]. Acta Metallurgica Sinica, 2024, 37 (1):54-66.
[18] Chellappa M, Vijayalakshmi U. Electrophoretic deposition of silica and its composite coatings on Ti-6Al4V, and its in vitro corrosion behaviour for biomedical applications [J]. Materials Science and Engineering: C, 2017, 71: 879-890.
[19] Xie K, Guo Y, Zhao S, et al. Partially melted Ti6Al4V particles increase bacterial adhesion and inhibit osteogenic activity on 3D-printed implants: an in vitro study [J]. Clinical Orthopaedics and Related Research,2019,477 (12): 2772- 2782.
[20] Guo Y, Ren L, Xie K, et al. Functionalized TiCu/ Ti-Cu-N-coated 3D-printed porous Ti6Al4V scaffold promotes bone regeneration through BMSC recruitment [J]. Advanced Materials Interfaces, 2020,7 (6): 1901632.
[21] Gao B, Zhao H, Peng L, et al. A review of research progress in selective laser melting (SLM)[J]. Micromachines, 2022, 14 (1): 57.
[22] Kolamroudi M K, Asmael M, Ilkan M, et al. Developments on electron beam melting (EBM) of Ti-6Al4V: a review [J]. Transactions of the Indian Institute of Metals, 2021, 74: 783-790.
[23] ÅłįŲ²łŻ¼äóĄ┬īÜŻ¼╚╬Ģį讯¼Ą╚ĪŻį÷▓─ųŲįņŌü║ŽĮ’@╬óĮYśŗš{┐ž┼c▒Ē├µĖ─ąį╝╝ągĄ─蹊┐▀Mš╣ [J]. ┴─│Ū┤¾īWīWł¾ (ūį╚╗┐ŲīW░µ), 2025,38 (4):543-553 ZHANG Yunlong, LIU Debao, REN Xiaoxue, et al. Research progress in microstructure control and surface modification of additive manufacturing titanium alloys [J]. Journal of Liaocheng University (Natural Science Edition), 2025, 38 (4): 543-553.
[24] ÅłįŲ²łŻ¼äóĄ┬īÜŻ¼╚╬Ģį讯¼Ą╚ĪŻ╗∙ė┌ TPMS ĮYśŗįOėŗĄ─Ōü║ŽĮį÷▓─ųŲįņ╝╝ągĄ─蹊┐▀Mš╣ [J/OL]. ┴─│Ū┤¾īWīWł¾ (ūį╚╗┐ŲīW░µ),.2025,38 (6):918-926. ZHANG Yunlong, LIU Debao, REN Xiaoxue, et al. Research progress of titanium alloy additive manufacturing technology based on TPMS structure designs [J]. Journal of Liaocheng University (Natural Science Edition), 2025,38 (6):918-926.
[25] Zhao X, Li S, Zhang M, et al. Comparison of the microstructures and mechanical properties of Ti-6Al-4V fabricated by selective laser melting and electron beam melting [J]. Materials & Design, 2016, 95: 21-31.
[26] Pasang T, Tavlovich B, Yannay O, et al. Directionally-dependent mechanical properties of Ti6Al4V manufactured by electron beam melting (EBM) and selective laser melting (SLM)[J]. Materials, 2021, 14 (13): 3603.
[27] Metalnikov P, Ben-Hamu G, Eliezer D. Corrosion behavior of AM-Ti-6Al-4V: A comparison between EBM and SLM [J]. Progress in Additive Manufacturing, 2022, 7 (3): 509-520.
[28] Bandekhoda M R, Mosallanejad M H, Atapour M, et al. Investigation on the potential of laser and electron beam additively manufactured Ti – 6Al – 4V components for orthopedic applications [J]. Metals and Materials International, 2024, 30 (1): 114-126.
[29] Zheng Y, Han Q, Wang J, et al. Promotion of osseointegration between implant and bone interface by titanium alloy porous scaffolds prepared by 3D printing [J]. ACS biomaterials science & engineering, 2020, 6 (9): 5181-5190.
[30] Bai Y, Gai X, Li S, et al. Improved corrosion behaviour of electron beam melted Ti-6Al – 4V alloy in phosphate buffered saline [J]. Corrosion Science, 2017, 123: 289-296.
[31] Martin Bezuidenhout, Elzaan Booysen, Anton Du Preez van Staden, et al.Selective Laser Melting of Integrated Ti6Al4V ELI Permeable Walls for Controlled Drug Delivery of Vancomycin [J]. ACS Biomaterials Science & Engineering,2018,4 (12): 4412-4424.
[32] Sun Z, Yin M, Sun Y, et al. Customized multilevel 3D printing implant for reconstructing spine tumor: a retrospective case series study in a single center [J]. Orthopaedic Surgery, 2022, 14 (9): 2016-2022.
[33] Luo X, Liu L H, Yang C, et al. Overcoming the strength–ductility trade-off by tailoring grain-boundary metastable Si-containing phase in β-type titanium alloy [J]. Journal of Materials Science & Technology, 2021, 68: 112-123.
[34] Ge Chen, Aikeremujiang Muheremu, Liu Yang, et al. Three-dimensional printed implant for reconstruction of pelvic bone after removal of giant chondrosarcoma: a case report [J].Journal of International Medical Research,2020, 48 (4): 1-10
[35] Yin C, Zhang T, Wei Q, et al. Surface treatment of 3D printed porous Ti6Al4V implants by ultraviolet photofunctionalization for improved osseointegration [J]. Bioactive Materials, 2022, 7: 26-38.
[36] Duan R, Li S, Cai B, et al. A high strength and low modulus metastable β Ti-12Mo-6Zr-2Fe alloy fabricated by laser powder bed fusion in-situ alloying [J]. Additive Manufacturing, 2021, 37: 101708.
[37] Tomaževič M, Kristan A, Kamath A F, et al. 3D printing of implants for patient-specific acetabular fracture fixation: an experimental study [J]. European Journal of Trauma and Emergency Surgery, 2021, 47: 1297- 1305.
[38] Drobniewski, Marek, et al. High Risk of Revision Associated with the L-Cup Titanium Alloy Porous Coated Acetabular Component in Primary Total Hip Arthroplasty: Minimum Follow-Up of 14 Years [J]. Journal of Clinical Medicine, 2025,14 (4 ): 1301.
[39] Ikumapayi, Omolayo M., et al. Finite Element Analysis and Simulation of 316L Stainless Steel and Titanium Alloy for Orthopedic Hip and Knee Prosthetics [J]. Prosthesis,2025, 7 (3): 64.
[40] Zhang H, Guo H P, Xu R D, et al. Surgical treatment outcomes of acetabular posterior wall and posterior column fractures using 3D printing technology and individualized custom-made metal plates: a retrospective study [J]. BMC surgery, 2024, 24: 157.
[41] Stoffelen D V C, Eraly K, Debeer P. The use of 3D printing technology in reconstruction of a severe glenoid defect: a case report with 2.5 years of follow-up [J]. Journal of Shoulder and Elbow Surgery, 2015, 24 (8): e218-e222.
[42] Arabnejad S, Johnston B, Tanzer M, et al. Fully porous 3D printed titanium femoral stem to reduce stressshielding following total hip arthroplasty [J]. Journal of Orthopaedic Research, 2017, 35 (8): 1774- 1783.
[43] Aherwar A., Patnaik A. & Bahraminasab M. Effect of Molybdenum Content on Structure and Properties of a Co-Cr Biomedical Alloy. J. of Materi Eng and Perform, 2019, 28: 6340–6353
[44] Singh, Ranjeet Kumar, and Swati Gangwar. An assessment of biomaterials for hip joint replacement [J]. International Journal of Engineering, Science and Technology, 2021,13 (1): 25-31.
[45] äó│┐Ż¼Åł┐╦Ż¼ŚŅ×IĪŻś╦£╩╗» 3D ┤“ėĪČÓ┐ūŌü║ŽĮ¾yŠ╩▒Ł╚½¾yĻP╣Øų├ōQągĄ─ųąŲ┌»¤ą¦ [J]. Ļæ▄Ŗ▄Ŗßt┤¾īWīWł¾Ż¼2022, 44 (15): 1538-1541 Liu Chen,Zhang Ke,Yang Bin. Mid-term efficacy of standardized 3D printed porous trabecular titanium acetabular cup in total hip arthroplasty [J]. Journal of Army Medical University, 2022, 44 (15): 15381541
[46] ═§Å®ĮŻ¼ų▄ėóĮ▄Ż¼═§ę·Ż¼Ą╚. 3D ┤“ėĪČÓ┐ūŌü║ŽĮūĄķg╚┌║ŽŲ„į┌ŅiūĄŪ░┬ĘūĄķg▒PŪą│²ų▓╣Ū╚┌║Žų╬»¤ŅiūĄ▓ĪągųąĄ─æ¬ė├ [J]. ųąć°╣Ū┼cĻP╣Øōpé¹ļsųŠŻ¼2023, 38 (1): 1-5. Wang Yanjin, Zhou Ying-jie, Wang Yin, et al Application of 3D print porous titanium alloy intervertebral fusion cage in anterior cervical discectomy and bone graft fusion for treatment of cervical spondylopathy [J].Chin J Bone Joint Injury, 2023,38 (1): 1-5
[47] Jingtao Ji, Guangdong Chen, Jun Miao. Preliminary Application of 3D-Printed Interbody Fusion Devices in the Treatment of Lumbar Degenerative Diseases [J]. 2024. https://doi.org/10.21203/rs.3.rs-4593148/v1.
[48] Huang Shuai, Jin Xuhui, Li Lei, et al. Biomechanical analysis of 3D printed porous extremely-low modulus Ti-24Nb-4Zr-8Sn lumbar interbody fusion cage-A finite element study [J]. Materials Technoloy, 2024, 39 (1): 2345960.
[49] Sun, Jun, et al. A lattice topology optimization of cervical interbody fusion cage and finite element comparison with ZK60 and Ti-6Al-4V cages [J].BMC musculoskeletal disorders,2021,22 (1): 390.
[50] McGilvray, Kirk C., et al. Bony ingrowth potential of 3D-printed porous titanium alloy: a direct comparison of interbody cage materials in an in vivo ovine lumbar fusion model [J]. The Spine Journal, 2018,18 (7): 1250-1260.
[51] Makino, Takahiro, et al. Comparison of short-term radiographical and clinical outcomes after posterior lumbar interbody fusion with a 3d porous titanium alloy cage and a titanium-coated PEEK cage [J]. Global Spine Journal, 2022,12 (5): 931-939.
[52] Christopher Donaldson, Tomislav Santro, Mohammed Awad, et al. 3D-printed titanium alloy cage in anterior and lateral lumbar interbody fusion for degenerative lumbar spine disease [J]. Journal of Spine Surgery, 2024, 10 (1): 22-30
[53] Runqi Xue, Qingguo Lai, Hongyu Xing, et al. Finite element analysis and clinical application of 3Dprinted Ti alloy implant for the reconstruction of mandibular defects [J]. BMC Oral Health, 2024, 24 (1): 95.
[54] Bingjing Zhao, Hong Wang, Changkui Liu, et al. A preliminary study of the mechanical properties of 3Dprinted personalized mesh titanium alloy prostheses and repair of hemi-mandibular defect in dogs [J]. Journal of Biomedical Materials Research Part B: Applied Biomaterials, 2024, 112 (9): e35466.
[55] Shi, Qimin, et al. Failure analysis of an in-vivo fractured patient-specific Ti6Al4V mandible reconstruction plate fabricated by selective laser melting [J]. Engineering Failure Analysis, 2021 (124): 105353.
[56] Dündar, Mehmet Akif, et al. Comparative biomechanical analysis of titanium fixation plates and NiTi shape memory staples for mandibular fracture treatment using finite element method [J]. Biomedical Signal Processing and Control ,2025 (103): 107501.
[57] Ban Ahmed Almudarris, Tanmay Rajput, Virendra Singh, et al. Outcomes of Using 3D-Printed Titanium Implants in Mandibular Reconstruction [J]. Journal of Pharmacy and Bioallied Sciences, 2025, 17: S1529- 1531.
[58] Hijazi, Khaled Marwan Anis. Porous Titanium Alloy Constructs for Mandibular Reconstruction. Electronic Thesis and Dissertation Repository. 2024:10292
[59] ÅłįŲ²łŻ¼äóĄ┬īÜŻ¼īO∙i’wŻ¼Ą╚ĪŻ╗∙ė┌ŽĪ═┴ōĮļsĄ─į÷▓─ųŲįņŌü║ŽĮ┴”īWąį─▄┼c╬óė^ĮM┐Śč▌╗»ÖCųŲ蹊┐ [J]. ┴─│Ū┤¾īWīWł¾ (ūį╚╗┐ŲīW░µ),2026,39 . https://doi.org/10.19728/j.issn1
Ż©ūóŻ¼įŁ╬─ś╦Ņ}Ż║į÷▓─ųŲįņŌü║ŽĮį┌╣Ū┐ŲųąĄ─æ¬ė├蹊┐▀Mš╣_ÅłįŲ²łŻ®
tagś╦║×:Ōü║ŽĮ,į÷▓─ųŲįņ,╣Ū┐Ųų▓╚ļ╬’,SLM╣ż╦ć,EBM╣ż╦ć



